
有关下列实验操作和相应的离子方程式的说法正确的是()
A. 等物质的量MgCl2、Ba(OH)2和HCl溶液混合:Mg2++3OH﹣+H+=Mg(OH)2↓+H2O
B. Ca(HCO3)2溶液与过量NaOH溶液反应:Ca2++HCO3﹣+OH﹣=CaCO3↓+2H2O
C. 等物质的量的FeBr2与Cl2反应为:2Fe2++2Br﹣+2Cl2=2Fe3++Br2+4Cl﹣
D. 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4﹣+6H++5H2O2=2Mn2++5O2↑+8H2O
考点: 离子方程式的书写.
分析: A.镁离子、氢离子与氢氧根离子发生反应,氢离子优先反应;
B.氢氧化钠过量反应生成碳酸钙、碳酸钠和水;
C.溴离子与二价铁离子具有还原性,二价铁离子还原性强于溴离子,氯气先氧化二价铁,再氧化溴离子;
D.浓盐酸可以被酸性高锰酸钾溶液氧化.
解答: 解:A.等物质的量MgCl2、Ba(OH)2和HCl溶液混合:Mg2++4OH﹣+2H+=Mg(OH)2↓+2H2O,故A错误;
B.Ca(HCO3)2与过量的NaOH溶液的反应的离子反应为Ca2++2HCO3﹣+2OH﹣=CaCO3↓+2H2O+CO32﹣,故B错误;
C.等物质的量的FeBr2和Cl2反应,亚铁离子优先反应,溴离子部分反应,反应的离子方程式为:2Fe2++2Br﹣+2Cl2═2Fe3++Br2+4Cl﹣,故C正确;
D.盐酸可以被酸性高锰酸钾溶液氧化,从而影响双氧水还原性的检验,故D错误;
故选:C.
点评: 本题考查了离子方程式的正误判断,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:原子个数是否守恒、电荷数是否守恒、化学式拆分是否正确、是否符合反应客观事实等,题目难度不大.


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000kJ•m﹣3的煤炭气,其主要成分是CO和H2.CO和H2可作为能源和化工原料,应用十分广泛.
(1)已知:
C(s)+O2(g)=CO2(g)△H1=﹣393.5kJ•mol﹣1 ①
2H2(g)+O2(g)=2H2O(g)△H2=﹣483.6kJ•mol﹣1 ②
C(s)+H2O(g)=CO(g)+H2(g)△H3=+131.3kJ•mol﹣1 ③
则反应CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g),△H= kJ•mol﹣1.标准状况下的煤炭气(CO、H2)33.6L与氧气完全反应生成CO2和H2O,反应过程中转移 mol e﹣.
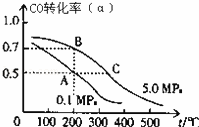
(2)密闭容器中充有10mol CO与20mol H2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g)⇌CH3OH(g);CO的平衡转化率(a)与温度、压强的关系如图所示.
①若A、B两点表示在某时刻达到的平衡状态,此时在A点时容器的体积为VAL,则该温度下的平衡常数K= ;A、B两点时容器中物质的物质的量之比为n(A)总:n(B)总= .
②若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA tC(填“大于”、“小于”或“等于”).
③在不改变反应物用量的情况下,为提高CO的转化率可采取的措施是 .
A 降温 B 加压 C 使用催化剂 D 将甲醇从混合体系中分离出来.
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等都离不开化学。
(1)硅是无机非金属材料的主角。请你举出两种含硅的材料名称________;铝制品表面因有一层氧化铝薄膜而经久耐用,但该氧化膜易被酸、碱破坏。若将氧化铝与氢氧化钠溶液作用,反应的离子方程式为________________________________________。
(2)氯气用于漂白时,实际上起漂白作用的物质不是Cl2而是它和水反应生成的________(写化学式)。缺铁性贫血患者补充的铁,通常以硫酸亚铁的形式,而硫酸铁则没有这种药效。当用硫酸亚铁制成药片时外表要包有一层特殊的糖衣,这层糖衣的作用是________________________________________________。
(3)从降低成本和减少环境污染的角度考虑,制取硫酸铜最好的方法是________(填选项字母)。
A.铜和浓硫酸反应
B.铜和稀硫酸反应
C.氧化铜和硫酸反应
D.铜与Fe2(SO4)3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质和应用均正确的是()
A. NH3能氧化氮氧化物,可用于汽车尾气净化
B. Mg、Fe等金属在一定条件下与水反应都生成H2和对应的氢氧化物
C. Fe在O2中的燃烧产物可用于制红色涂料
D. Mg (OH)2分解吸热且生成高熔点固体,可用作阻燃剂
查看答案和解析>>
科目:高中化学 来源: 题型:
在化学学习中使用数轴的表示方法可收到直观、形象的效果,下列表达中正确的是()
A. 分散质微粒的大小与分散系种类的关系: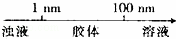
B. 常温下溶液的pH其酸碱性的关系: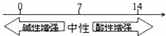
C. 硫的化合物中化合价与其氧化性、还原性的关系: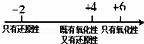
D. Fe在Cl2中燃烧的产物与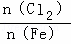 的关系:
的关系:
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42﹣、HCO3﹣等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是()
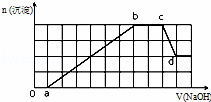
A. 原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
B. ab段发生的离子反应为:Al3++3OH﹣=Al(OH)3↓,Mg2++2OH﹣=Mg(OH)2↓
C. 原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+、Na+
D. d点溶液中含有的溶质只有Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组的学生根据活泼金属Mg与CO2发生反应,推测活泼金属钠也能与CO2发生反应,因此兴趣小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去).已知:常温下,CO能使一些化合物中的金属离子还原
例如:PdCl2+CO+H2O=Pd↓+CO2+2HCl.反应生成黑色的金属钯,此反应也可用来检测微量CO的存在.
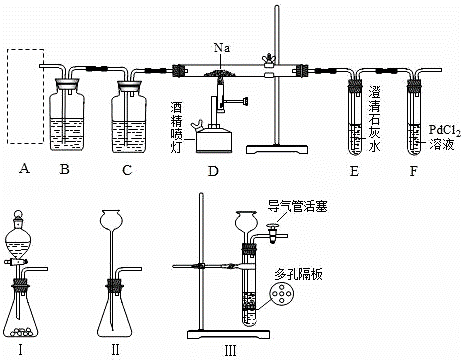
请回答下列问题:
(1)通常实验室制取CO2气体的离子方程式是,为了使制气装置能“随开随用,随关随停”,上图A处应选用的装置是Ⅲ(填写“Ⅰ”、“Ⅱ”或“Ⅲ”).若要制取干燥、纯净的CO2气体,装置B、C中各盛放的试剂分别为饱和、.
(2)装入药品后,在点燃酒精喷灯前,必须进行的操作是通.待装置填写字母)中出现浑浊现象时,再点燃酒精喷灯,这步操作的目的是.
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:
①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是.
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式(需注明正确的反应条件)是.
(4)请用文字简要说明你判断②中D装置生成固体的成分是钠的正盐还是酸式盐生成正盐理由:.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y均为1~18号之间的元素,X、Y可形成化合物X2Y和X2Y2,又知Y的原子序数小于X的原子序数,则这两种元素的原子序数之和为()
A. 19 B. 18 C. 16 D. 9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com