
| A. | 氯气和水发生反应:Cl2+H2O?2H++Cl-+ClO- | |
| B. | 用NaOH溶液除去铝表面的氧化膜时产生气泡:2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑ | |
| C. | 金属钠和水反应:Na+2H2O=Na++2OH-+H2↑ | |
| D. | 将铁粉加入稀硫酸和硝酸钾混合溶液中,铁粉溶解:Fe+2H+=Fe2++H2↑ |
分析 A.次氯酸为弱酸,不能拆;
B.氯气与氢氧化钠溶液反应生成四羟基合铝酸钠和氢气;
C.电荷不守恒;
D.硝酸具有强的氧化性,与任何金属反应都不生成氢气.
解答 解:A.氯气和水发生反应,离子方程式:Cl2+H2O?H++Cl-+HClO,故A错误;
B.氯气与氢氧化钠溶液反应生成四羟基合铝酸钠和氢气,离子方程式:2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑,故B正确;
C.金属钠和水反应,离子方程式:2Na+2H2O=2Na++2OH-+H2↑,故C错误;
D.硝酸具有强的氧化性,与任何金属反应都不生成氢气,故D错误;
故选B.
点评 本题考查离子反应方程式的正误判断,明确发生的化学反应及离子反应的书写方法即可解答,注意化学式的拆分,注意离子反应遵循客观事实,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 与等体积pH=11的NaOH溶液混合后所得溶液显酸性 | |
| B. | c(H+)=c(CH3COO-)+c(OH-) | |
| C. | 该溶液中由水电离出的c(H+)是1.0×10-11 mol/L | |
| D. | 加入少量CH3COONa固体后,c(CH3COO-)降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
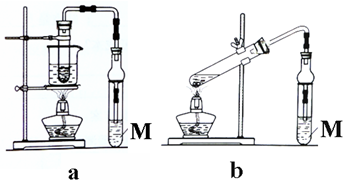
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL 1mol/LAlCl3溶液 | B. | 200 mL 1mol/LMgCl2溶液 | ||
| C. | 100mL 0.5mol/LCaCl2溶液 | D. | 100 mL 2 mol/L KCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 适当升高温度 | B. | 加入NH4Cl固体 | C. | 通入NH3 | D. | 加水稀释 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 水电离的[H+]随着温度的升高而降低 | B. | 在35℃时,水电离的[H+]>[OH-] | ||
| C. | 水的电离程度:35℃>25℃ | D. | 水电离的[OH-]随温度升高而增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com