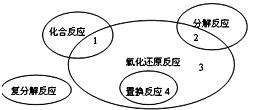
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于3 区域的是
| △
练习册系列答案
相关习题
科目:高中化学
来源:
题型:
(2011?淮南二模)A、B、C、D四种短周期元素,原子序数依次增大,原子半径按C、D、B、A顺序逐渐减小.A、C同主族,B、D同主族;A、C的原子核内质子数之和为B、D的原子核内质子数之和的一半;C元素与其它三种元素均能形成离子化合物.试回答下列问题: (1)B的离子符号 O2- O2- ;D基态原子的核外电子排布式 1S22S22P63S23P4 1S22S22P63S23P4 ;C、D形成化合物的电子式 ; (2)同时含有上述四种元素的化合物有多种,试写出其中两种的化学式(要求:其中有一种水溶液显中性) Na2SO4?10H2O Na2SO4?10H2O 、 NaHSO4(或NaHSO3) NaHSO4(或NaHSO3) ; (3)A、B、C三元素中各由两种组成的两种化合物,相互反应生成A的单质的化学方程式为 NaH+H2O═NaOH+H2↑ NaH+H2O═NaOH+H2↑ ; (4)B、C、D三元素中各由两种组成的两种化合物,发生化合反应且属于氧化还原反应的化学方程式为 Na2O2+SO2═Na2SO4 Na2O2+SO2═Na2SO4 .
查看答案和解析>>
科目:高中化学
来源:
题型:
有甲基、苯基、羟基、羧基四种基团,在它们两两组合形成的化合物中,写出具有以下性质的物质的结构简式: (1)能使石蕊试液变色的是 CH3COOH(C6H5COOH、H2CO3) CH3COOH(C6H5COOH、H2CO3) (任写一种). (2)能与溴水发生取代反应的是 C6H5OH C6H5OH . (3)催化氧化后产物能与新制氢氧化铜发生氧化还原反应的是 CH3OH CH3OH . (4)能与氯化铁溶液发生显色反应的是 C6H5O C6H5O . (5)不同情况下与氢氧化钠反应能生成两种盐的是 H2CO3 H2CO3 .
查看答案和解析>>
科目:高中化学
来源:
题型:
有甲基、苯基、羟基、羧基四种基团,在它们两两组合形成的化合物中,写出具有以下性质的物质的结构简式: (1)能使石蕊试液变色的是 CH 3COOH、  或HOCOOH CH 3COOH、  或HOCOOH (任写一种). (2)能与溴水发生取代反应的是 . (3)催化氧化后产物能与新制氢氧化铜发生氧化还原反应的是 CH3OH CH3OH . (4)能与氯化铁溶液发生显色反应的是 .
查看答案和解析>>
科目:高中化学
来源:
题型:
 (2011?江苏)原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29. 回答下列问题: (1)Y 2X 2分子中Y原子轨道的杂化类型为 sp杂化 sp杂化 ,1mol Y 2X 2含有σ键的数目为 3mol或3×6.02×1023个 3mol或3×6.02×1023个 . (2)化合物ZX 3的沸点比化合物YX 4的高,其主要原因是 NH3分子存在氢键 NH3分子存在氢键 . (3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是 N2O N2O . (4)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是 CuCl CuCl ,它可与浓盐酸发生非氧化还原反应,生成配合物H 2WCl 3,反应的化学方程式为 CuCl+2HCl═H2CuCl3(或CuCl+2HCl═H2[CuCl3] CuCl+2HCl═H2CuCl3(或CuCl+2HCl═H2[CuCl3] .
查看答案和解析>>
科目:高中化学
来源:
题型:阅读理解
[化学--选修3:物质结构与性质]X、Y、Z、W是元素周期表中前四周期中的四种元素,其中X的原子中不存在中子,Y原于的最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.请回答下列问题: 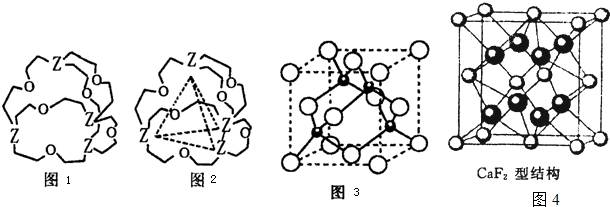 (1)写出Y原子基态时的价电子排布式: . (2)X和Y可以形成Y 2X 4分子,1个Y 2X 4分子中含有σ键的数目为 ,其中Y原子的杂化轨道类型为 . (3)元素Y的一种氧化物与元素2的一种氧化物互为等电子体,则元素Z的这种氧化物的分子式是 . (4)图1表示某种含Z有机化合物的结构,其分子内4个Z原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别.下列分子或离子中,能被该有机化合物识别的是 (填标号). A.CF 4 B.CH 4 C.NH D.H 2O (5)元素W的一种氯化物晶体的晶胞结构如图3所示,该氯化物的化学式是 .已知其晶胞边长为a nm,则其晶体密度为 g?cm -3(列出算式即可).该氯化物可与浓盐酸发生非氧化还原反应,生成配合物H nWCl 3,则反应的化学方程式为 . (6)元素金(Au)与W形成的一种合金晶体具有立方最密堆积的结构,在晶胞中W原子处于面心,Au原子处于顶点位置.该晶体中原子之间的作用力是 ;该晶体具有储氢功能,氢原子可进入到由W原子与Au原子构成的四面体空隙中.若将W原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF 2的结构图4相似,该晶体储氢后的化学式应为 .
查看答案和解析>>
| |

