
下列说法正确的是
A.同周期X、Y、Z元素的最高价含氧酸的酸性:HXO4>H2YO4>H3ZO4,则气态氢化物还原性HX<H2Y<ZH3
B.元素R的含氧酸的化学式是H2RO3,则其气态氢化物的化学式就是RH4
C.金属与非金属元素分界线附近的元素是过渡元素
D.物质的量相同的Na+、O2-、NH3三种微粒,一定含有相同的质子
科目:高中化学 来源:2015-2016学年江苏省江阴市高二下期中化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.常温下,将醋酸稀溶液加水稀释,溶液中c(H+)/c(CH3COOH)增大
B.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应
C.反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的△H>0
D.25℃时、用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆石河子二中高二下学期第二次月考化学试卷(解析版) 题型:选择题
下列有机物不能使酸性高锰酸钾褪色的是( )
A.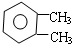 B.邻甲基苯酚 C.
B.邻甲基苯酚 C.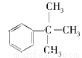 D.2-甲基-2-己烯
D.2-甲基-2-己烯
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆石河子二中高二下学期第二次月考化学试卷(解析版) 题型:选择题
CH2=CHCH=CH2与Br2 按照1:1比例反应,产物可能是 ( )
A.CH2=CHCH(Br)CH2Br B.CH2=CH(Br)CHCH2Br
C.CH2=CH2CH2CHBr2 D.CH Br2CH=CHCH3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市静海县六校高一下学期期中联考化学试卷(解析版) 题型:实验题
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果:_______与盐酸反应最剧烈,______与盐酸反应最慢。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理_______说明理由:_____________________________。
Ⅱ.利用下图装置可以验证非金属性的变化规律。
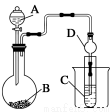
(3)仪器A的名称为____,干燥管D的作用是______________。
(4) 实验验证氯的非金属性大于硫:A中放浓盐酸、B中放KMnO4、C中盛放__________,离子方程式为____________。从环境保护的观点考虑,此装置缺少尾气处理装置,可用________溶液吸收尾气.
(5)若要证明非金属性:C>Si,则A中加盐酸、B中加Na2CO3、C中加________,观察到C中溶液的现象为____________________。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有________溶液的洗气瓶.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市静海县六校高一下学期期中联考化学试卷(解析版) 题型:选择题
可逆反应2NO2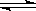 2NO+O2在恒容密闭容器中进行,下列情况达到平衡状态的是
2NO+O2在恒容密闭容器中进行,下列情况达到平衡状态的是
①内生成n mol O2的同时生成2n mol NO2 ②合气体的平均相对分子质量不再改变
③O2、NO、O2的反应速率之比为2∶2∶1 ④合气体的颜色不再改变
⑤合气体的密度不再改变 ⑥合气体压强不再改变
A.①②④ B.②③⑤ C.①②⑤⑥ D.①②④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市静海县六校高一下学期期中联考化学试卷(解析版) 题型:选择题
下列有关化学反应速率的说法正确的是
A.用铁片和稀硫酸反应制氢气时,可改用98%的浓硫酸加快生成氢气速率
B.100 mL2mol·L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C.SO2的催化氧化是一个放热反应,所以升高温度,反应速率减慢
D.汽车尾气中NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率减慢
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市静海县六校高二下学期期中联考化学试卷(解析版) 题型:选择题
可以把5种无色溶液:乙醇、苯酚、Na2CO3溶液、AgNO3溶液、KOH溶液一一区分的试剂是
A.新制碱性Cu(OH)2悬浊液 B.FeCl3溶液
C.BaCl2溶液 D.酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省实验学校高二下期中化学试卷(解析版) 题型:填空题
t℃时,将3 mol A 和1 mol B气体,通入体积为2L的密闭容器(容积不变),发生反应:3A(g) + B(g)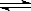 4 C(g) 2min时反应达到平衡状态(温度不变),并测得C 的浓度为0.4 mol/L,请填写下列空白:
4 C(g) 2min时反应达到平衡状态(温度不变),并测得C 的浓度为0.4 mol/L,请填写下列空白:
(1)从反应开始到达到平衡状态,生成C的平均反应速率为_________________。
(2)达到平衡状态时, B 物质的转化率α(B) = _____________,平衡常数K= __________________(填计算结果)。
(3)若继续向原混和物质通入少量氦气后(设氦气不与A、B、C反应),化学平衡_________
A、向正反应方向移动 B、向逆反应方向移动 C、平衡不移动
(4)若向原平衡中再充入a mol C,在t℃时达到新平衡,此时B的物质的量为:n (B) = ________________ mol.
(5)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间该满足的关系为:_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com