
下列反应中,离子方程式书写正确的是
A.Fe和盐酸反应:2Fe + 6H+= 2Fe3++3H2↑
B.Cu和AgNO3溶液反应:Cu +Ag+= Cu2++ Ag
C.石灰石和盐酸反应: CO32-+ 2H+ = CO2↑+ H2O
D.氢氧化钡与盐酸反应: OH- + H+= H2O
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
在1 L HNO3和H2S04的混合溶液中,两种酸的物质的量浓度之和为O.6 mol/l,向该溶液中加入足量铜粉,加热,充分反应,当HNO3与H2S04的物质的量比为x:y 时所得溶液中Cu2+物质的量浓度最大,则x:y为
A.3:8 B.2:3 C.1:4 D.1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是学习化学的重要工具,下列化学用语中,正确的是( )
A、电解饱和食盐水时,阳极的电极反应式为:2Cl- -2e-= Cl2 ↑
B、氢氧燃料电池的负极反应式:O2 + 2H2O + 4e- = 4OH-
C、镀件上电镀铜时,纯铜做阴极,电极反应式为:Cu -2e- = Cu2+
D、钢铁发生电化学腐蚀的正极反应式:Fe-2e- = Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
二甲醚(CH3OCH3)被称为21世纪界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)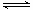 CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1
②2CH3OH(g)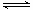 CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
③CO(g)+H2O(g)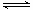 CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1
(1)若要增大反应①中H2的转化率,在其它条件不变的情况下可以采取的措施为 。
A.加入某物质作催化剂 B.加入一定量CO C.反应温度降低 D.增大容器体积
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1 mol/L,c(H2)=2 mol/L,5 min后达到平衡,CO的转化率为50%,则5 min内CO的平均反应速率
为 ;
若反应物的起始浓度分别为:c(CO)=4 mol/L,c(H2)=a mol/L;达到平衡后,c(CH3OH)=2 mol/L,a= mol/L。
(3)催化反应室中总反应3CO(g)+3H2(g)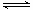 CH3OCH3(g)+CO2(g)的△H= 。
CH3OCH3(g)+CO2(g)的△H= 。
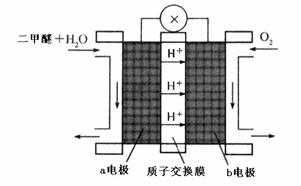
(4)“二甲醚燃料电池”是一种绿色电源,其工作原理如上图所示。b电极是 极,写出b电极上发生的电极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有以下物质 ① NaNO3溶液 ② 熔融的MgCl2 ③CuSO4粉末 ④ NaOH 固体
⑤ 金属铜 ⑥ 蔗糖。 有关它们的说法正确的是
A. 能导电的有①②③④⑤; B. 属于电解质有①②③④
C. 不能导电的有③④⑥ D. 属于纯净物的只有④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学为了测定三聚氰胺的分子式,设计了如下实验:
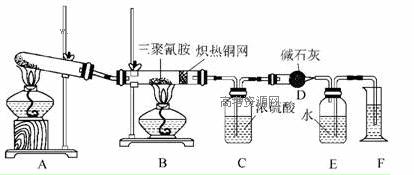
查阅资料,三聚氰胺的相对分子质量为126,在常温下为晶体,由碳、氢、氮三种元素组成,加热条件下能与氧气发生反应生成二氧化碳、氮气和水。取12.6 g三聚氰胺晶体按图示实验装置进行三聚氰胺与氧气的反应(假设三聚氰胺完全转化成产物),并通过测定生成物的量计算三聚氰胺的分子组成。
(1)写出A装置中发生反应的化学方程式_______________________________________。
(2)C装置能不能与D装置互换?__________(填“能”或“不能”)。理由是__________________________。
(3)当B装置中反应完全发生后,读取F中水的体积的实验操作顺序为__________(填序号)。
①读数 ②冷却至室温 ③调平E、F装置中的液面
(4)测定数据如下:
| 装置 | C | D |
| 实验前 | 101.0 g | 56.0 g |
| 实验后 | 106.4 g | 69.2 g |
经测定,E中收集的气体折合成标准状况下的体积为6.72 L。
①利用上述实验数据,计算三聚氰胺的分子式为__________。
②若B装置中没有铜网,对测定结果的影响是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列依据热化学方程式得出的结论正确的是( )
A.已知2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ· mol-1说明2 mol H2(g)和1 mol O2(g)的能量总和小于2 mol H2O(g)的能量
B.已知C(s,石墨)===C(s,金刚石) ΔH>0,则金刚石比石墨稳定
C.已知NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1,
则含20 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量
D.已知2C(s)+2O2(g)===2CO2(g) ΔH1
2C(s)+O2(g)===2CO(g) ΔH2,则ΔH1>ΔH2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com