
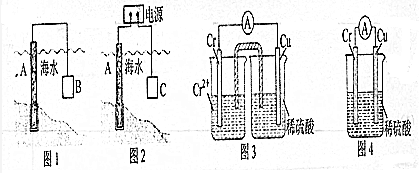
分析 (1)形成原电池时,Fe作正极被保护;电解池中Fe作阴极被保护;C为阳极,阳极接石墨,不需要频繁更换;
(2)①Cr比铜活泼,Cr为负极,Cu为正极,正极上氢离子得电子;
A、盐桥中不是都可以用饱和KCl琼脂溶液,要考虑能否与电解质溶液反应;
B、1molCr反应,转移2mol电子;
C、氢离子得电子发生还原反应;
D、盐桥中是离子移动,无电子通过;
②正极上是硝酸根离子得电子生成NO,结合电荷守恒和原子守恒书写电极反应式;
(3)根据发生的电极反应,可以知道金属铁是阴极,石墨电极是阳极,根据电解质中离子的放电顺序以及电极反应和电子的转移知识来回答即可.
解答 解:(1)原电池原理保护金属铁时,将铁与比铁活泼的金属相连,属于牺牲阳极的阴极保护法;电解池原理保护金属铁时,铁作阴极,阳极接石墨,不需要频繁更换;
故答案为:牺牲阳极的阴极保护法;d;
(2)①Cr比铜活泼,Cr为负极,Cu为正极,正极上氢离子得电子,所以铜电极上有气泡生成;
A、盐桥中不是都可以用饱和KCl琼脂溶液,若电解质溶液为硝酸银溶液时,会生成沉淀,故A错误;
B、1molCr反应,转移2mol电子,为保持电荷守恒,盐桥中将有2molCl-进入左池,2molK+进入右池,故B正确;
C、氢离子得电子发生还原反应,故C错误;
D、盐桥中是离子移动,无电子通过,故D错误;
故答案为:铜电极上有气泡产生;B;
②正极上是硝酸根离子得电子生成NO,有氢离子参与反应,电极反应式为:4H++NO3-+3e-=NO↑+2H2O,
故答案为:4H++NO3-+3e-=NO↑+2H2O;
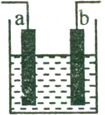
(3)①根据发生的电极反应,可以知道金属铁是阴极,接电源的负极,故答案为:负极;
②阴极上氢离子放电发生还原反应,生成氢气,阳极发生氧化反应,阳极的电极反应式为:CN--2e-+2OH-═CNO-+H2O和2Cl--2e-═Cl2↑,
故答案为:氢气;CN--2e-+2OH-═CNO-+H2O.
点评 本题考查了原电池原理和电解池原理的分析应用,把握原电池原理和电解池原理以及电解过程中电子的移动方向,掌握基础是关键,题目难度中等,侧重于考查学生的分析能力.


科目:高中化学 来源: 题型:选择题
| 选项 | 操作及现象 | 结论 |
| A | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 | 溶液中含有NH4+ |
| B | 将浓硝酸滴入碳酸钠溶液中,然后将生成的气体直接通入硅酸钠溶液中,溶液变浑浊. | 酸性:硝酸>碳酸>硅酸 |
| C | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,溶液变成蓝色 | 氧化性:I2>Cl2 |
| D | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
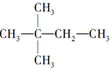 ,则A的结构简式为(CH3)3CCH=CH2.
,则A的结构简式为(CH3)3CCH=CH2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
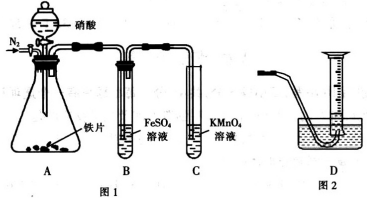 为探究铁和稀硝酸反应的产物,某兴趣小组进行如下实验.
为探究铁和稀硝酸反应的产物,某兴趣小组进行如下实验.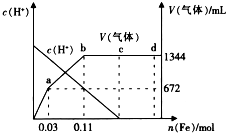
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是国际单位制中七个基本物理量之一 | |
| B. | 摩尔是物质的量的单位,简称摩,符号为mol | |
| C. | 摩尔可以把物质的宏观数量与微观粒子的数量联系起来 | |
| D. | 国际上规定,0.012 kg碳原子中所含有的碳原子数目为1摩 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4- Cl- | Cl2、Mn2+ |
| A. | 第①组反应的其余产物为H2O和 O2 | |
| B. | 第②组反应从产物结果可以得出还原性顺序:Fe2+>Br- | |
| C. | 第③组反应中生成1mol Cl2,转移电子数为2NA | |
| D. | 氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝 | B. | 硅 | C. | 金刚石 | D. | 硫 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com