
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
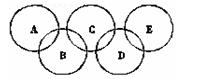
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


A.由于水中存在氢键,所以稳定性:H2O>H2S | B.由于Cl的非金属性比S的非金属性强,所以酸性:HClO>H2SO4 |
C.若A2 + 2D— ="=" 2A— + D2,则氧化性D2>A2 | D.若R2—和M+的电子层结构相同,则离子半径R2—>M+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 液并使它们接近,有大量白烟生成;甲为一种淡黄色固体,D、F的溶液均呈碱性。则
液并使它们接近,有大量白烟生成;甲为一种淡黄色固体,D、F的溶液均呈碱性。则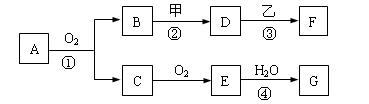
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素的非金属性:X>Y>Z |
| B.阴离子的还原性:X<Y<Z |
| C.气态氢化物的稳定性:X>Y>Z |
| D.最高价氧化物的水化物的酸性:Z>Y>X |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com