
向NaOH和Na2CO3混合溶液中滴加0.1mol/L稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示。下列判断正确的是

A.在0-a范围内,只发生中和反应
B.ab段发生反应的离子方程式为:CO32-+2H+=H2O+CO2↑
C.a=0.3
D.原混合溶液中NaOH与Na2CO3的物质的量之比为1:2
C
【解析】
试题分析: 向NaOH和Na2CO3混合溶液中滴加0.1mol/L稀盐酸发生的反应依次为H++OH-=H2O、CO32-+H+=HCO3-、HCO3-+H+=H2O+CO2↑,据此可以解答。A、在0-a范围内,发生的反应应该是H++OH-=H2O、CO32-+H+=HCO3-、,不止有中和反应,A不正确;B、ab段发生反应的离子方程式为HCO3-+H+=H2O+CO2↑,B不正确;C、生成CO2的物质的量是0.1mol,则根据方程式HCO3-+H+=H2O+CO2↑可知,消耗盐酸的物质的量是0.1mol,所以a=0.3,C正确;D、根据方程式和图像可知碳酸钠的物质的量是0.1mol,共计消耗盐酸是0.2mol,所以与氢氧化钠反应的盐酸是0.4mol-0.2mol=0.2mol,则氢氧化钠的物质的量是0.2mol,因此原混合溶液中NaOH与Na2CO3的物质的量之比为2:1,D不正确,答案选C。
考点:考查氢氧化钠、碳酸钠与盐酸反应的有关计算以及图像分析与判断


科目:高中化学 来源: 题型:
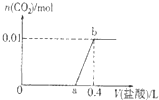 向NaOH和Na2CO3混合溶液中滴加0.1mol?L-1稀盐酸,CO2的生成量与加入盐
向NaOH和Na2CO3混合溶液中滴加0.1mol?L-1稀盐酸,CO2的生成量与加入盐| A、在0-a范围内,只发生中和反应 | ||
B、ab段发生反应的离子方程式为:CO
| ||
| C、a=0.3 | ||
| D、原混合溶液中NaOH与Na2CO3的物质的量之比为1:2 |
查看答案和解析>>
科目:高中化学 来源:2014届度辽宁大连瓦房店中学高一上学期期末考试化学试卷 题型:选择题
向X的溶液中,加入Y试剂,产生的沉淀或气体如图所示与所述情形相符的是( )
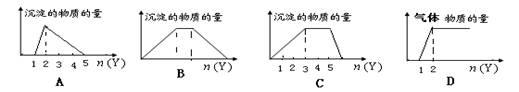
A. 向HCl和AlCl3的混合液中滴加NaOH
B.向NaOH和Ca(OH)2的混合液中通入CO2
C.向NH4Al(SO4)2溶液中滴加NaOH
D.向NaOH和Na2CO3的混合液中滴加稀HCl
查看答案和解析>>
科目:高中化学 来源:2010-2011学年辽宁省葫芦岛一高高一(上)月考化学试卷(解析版) 题型:选择题
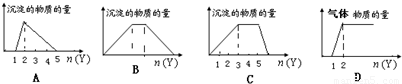
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com