
 1mol·L-1的NaOH溶液的pH为11,则该温度下水的Kw= .(2分)
1mol·L-1的NaOH溶液的pH为11,则该温度下水的Kw= .(2分)科目:高中化学 来源:不详 题型:填空题
 。
。
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 (偏高、偏低或无影响)。
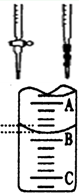
(偏高、偏低或无影响)。 管中的液面,右图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为 mL。
管中的液面,右图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为 mL。| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.52 | 25.42 |
| 第二次 | 20.00 | 4.07 | 29.17 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2C4H10+13O2 ="=" 8CO2+10H2OΔH=-5 753.6 kJ·mol-1 |
| B.C4H10(g)+13/2 O2(g)==4CO2(g)+5H2O(g)ΔH=-2 876.8 kJ·mol-1 |
| C.2C4H10(g)+13O2(g)==8CO2(g)+10H2O(l)ΔH=-2 876.8 kJ·mol-1 |
| D.C4H10(g)+13/2 O2(g)==4CO2(g)+5H2O(l)ΔH=-2 876.8 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 液中,以0.50 mol/L氢氧化钠溶液滴定后得滴定曲线如图所示。
液中,以0.50 mol/L氢氧化钠溶液滴定后得滴定曲线如图所示。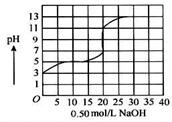
A.该弱酸在滴定前 的浓度是0.15 mol/L 的浓度是0.15 mol/L |
| B.该弱酸稀释10倍后pH为4 |
| C.滴定过程为求滴定终点,最合适的指示剂是酚酞 |
| D.滴定过程为求滴定终点,最合适的指示剂是甲基橙 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 OH-)为
OH-)为| A.2.0×10-7 mol·L-1 | B.0.1×10-7 mol·L-1 |
| C.1.0×10-14/2.0×10-7 mol·L-1 | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com