

| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.6 | 9.0 | -- | -- |
| 沉淀完全时的pH | 3.7 | 9.6 | 11.0 | 8(>8溶解) | 9(>9溶解) |

分析 铬铁矿用稀硫酸酸浸,FeO、Cr2O3、MgCO3、Al2O3与硫酸反应加入溶液,而SiO2不反应,过滤除去SiO2.用H2O2将Fe2+氧化为Fe3+,再调节pH=8时,Fe3+、Al3+完全沉淀,过滤得到滤渣为Al(OH)3和Fe(OH)3,再调节pH>11,Mg2+完全沉淀被除去且Cr元素以CrO2-的形式存在,过滤后,向滤液中再加入过氧化氢,将CrO2-氧化为CrO42-,最后采取蒸发浓缩、冷却结晶的方法得到Na2CrO4晶体.
(1)流程中第一次过滤后滤渣的主要成分是SiO2,第一次加入H2O2是为了将Fe2+氧化为Fe3+,第二次加入H2O2是为了将CrO2-氧化为CrO42-;
(2)“调pH=8”时沉淀成分是Al(OH)3和Fe(OH)3,如果不把前者除去,当继续加入NaOH至pH=11时,Al(OH)3会溶解,引入杂质离子AlO2-;
(3)Na2CrO4溶液得到Na2CrO4晶体,可以采取蒸发浓缩、冷却结晶的方法;
(4)①反应(I)Cr2O72-转化为Cr3+,亚铁离子被氧化为铁离子,依据化学反应的元素化合价变化结合电子守恒、电荷守恒、原子守恒书写离子方程式;
②根据$\frac{C(F{e}^{3+})}{C(C{r}^{3+})}$=$\frac{{k}_{sp}[Fe(OH)_{3}]}{{K}_{sp}[Cr(OH)_{3}]}$,计算废水中c(Fe3+);
(5)①溶液中有碘,加入淀粉溶液呈蓝色;
②根据反应的关系式计算.
解答 解:(1)铬铁矿用稀硫酸酸浸,FeO、Cr2O3、MgCO3、Al2O3与硫酸反应加入溶液,而SiO2不反应,过滤除去SiO2,第一次加入H2O2是为了将Fe2+氧化为Fe3+,反应离子方程式为:2Fe2++H2O2+2H+═2Fe3++2H2O;第二次加入H2O2是为了将CrO2-氧化为CrO42-,反应离子方程式为:2CrO2-+3H2O2+2OH-═2CrO42-+4H2O,
故答案为:SiO2;2CrO2-+3H2O2+2OH-═2CrO42-+4H2O;
(2)“调pH=8”时沉淀成分是Al(OH)3和Fe(OH)3,如果不把前者除去,当继续加入NaOH至pH=11时,Al(OH)3会溶解,引入杂质离子AlO2-,
故答案为:pH>11时Al(OH)3会溶解,引入杂质离子AlO2-,使产品不纯;
(3)Na2CrO4溶液得到Na2CrO4晶体,可以采取蒸发浓缩、冷却结晶的方法,涉及到的操作有蒸发浓缩、冷却结晶、过滤、洗涤、干燥等,
故答案为:蒸发浓缩、冷却结晶、过滤、洗涤、干燥;
(4)①反应(I)Cr2O72-转化为Cr3+,亚铁离子被氧化为铁离子,电子转移:Cr2O72-~2Cr3+~6e-;6Fe2+~6Fe3+~6e-,所以配平氧化还原反应的电子守恒,结合电荷守恒和原子守恒得到离子方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,
故答案为:Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O;
②由Ksp Fe(OH)3=4.0×10-38,KspCr(OH)3=6.0×10-31,已知电解后的溶液中c(Cr3+)为3×10-6mol•L-1,由$\frac{C(F{e}^{3+})}{C(C{r}^{3+})}$=$\frac{{k}_{sp}[Fe(OH)_{3}]}{{K}_{sp}[Cr(OH)_{3}]}$,则溶液中c(Fe3+)=$\frac{4.0×1{0}^{-38}}{6.0×1{0}^{-31}}$×3×10-6mol/L=2×10-13mol/L,
故答案为:2×10-13;
(5)①溶液中有碘,加入淀粉溶液呈蓝色,碘与亚硫酸钠发生氧化还原反应,当反应终点时,蓝色褪去,
故答案为:当滴加最后一滴硫代硫酸钠溶液时,溶液蓝色褪去,半分钟内不变色;
②根据反应的关系式计算:
Cr2O72-~3I2~6S2O32-
1mol 6mol
n 0.1200mol•L-1×0.04L
n=0.0008mol,则2.5000g重铬酸钠试样中含有的重铬酸钠的质量为10×0.0008mol×262g/moL=2.096g,
所得产品的中重铬酸钠的纯度=$\frac{2.096}{2.500}$×100%=83.84%,
故答案为:83.84%.
点评 本题属于工艺流程制备题目,考查制备原理、实验方案评价、物质分离提纯、计算能力、获取信息的能力,是对基础知识的综合考查,注意(5)从氧化还原反应的角度分析,题目难度中等.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ①②③⑥ | C. | ③④⑤⑥ | D. | ①④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与W可以形成W2X、W2X2两种化合物 | |
| B. | Y元素最高价氧化物对应水化物的化学式为H2YO4 | |
| C. | X、Y、Z对应氢化物的热稳定性和还原性强弱顺序一致 | |
| D. | Y、Z两元素的简单离子的半径Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 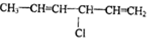 | B. | 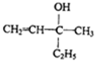 | ||
| C. | 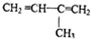 | D. | 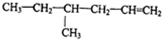 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +(2n-1)H2O
+(2n-1)H2O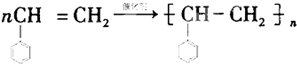
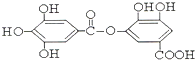 与NaOH的反应
与NaOH的反应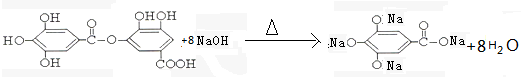
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
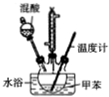 2-硝基甲苯和4-硝基甲苯均可用于印染行业,实验室利用下列反应和装置制备这两种物质
2-硝基甲苯和4-硝基甲苯均可用于印染行业,实验室利用下列反应和装置制备这两种物质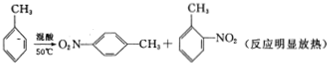
| 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解性 | |
| 甲苯 | 92 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
| 2-硝基甲苯 | 137 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
| 4-硝基甲苯 | 137 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
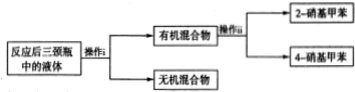
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
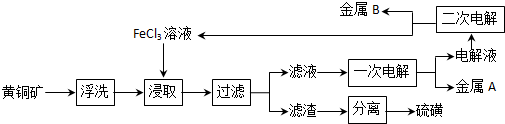
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有共价键的晶体,一定是原子晶体 | |
| B. | 离子晶体中,一定存在金属元素和非金属元素 | |
| C. | 同时含有离子键和共价键的化合物,既可能是离子化合物,也可能是共价化合物 | |
| D. | 在共价化合物中一定存在共价键,但含有共价键的不一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
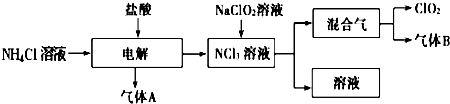
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com