
���� ��1������C�����ʵ������㷴Ӧ��A�����ʵ������Ӷ�֪��Ϊ��Ӧ��A�����ʵ�����������Ũ�ȹ�ʽ���㣻
��2������C�����ʵ������㷴Ӧ��B�����ʵ��������ݷ�Ӧ���ʹ�ʽ���㣻
��3������ͬһ��Ӧ�С�ͬһʱ����ڣ������ʵķ�Ӧ����֮�ȵ��ڼ�����֮��ȷ��nֵ��
��4���Ѳ�ͬ���ʵķ�Ӧ���ʻ����ͬһ���ʵķ�Ӧ���ʽ��бȽϣ�
��� �⣺��1��A��g��+2B��g��?3C��g��+nD��g����
��Ӧ��ʼ 4mol 6mol 0 0
��Ӧ 1 mol 2 mol 3 mol
5minĩ 3 mol 4mol 3 mol
C��A��=$\frac{n}{V}$=1.5 mol/L
�ʴ�Ϊ��1.5 mol/L��
��2��v��B��=$\frac{��n}{V��t}$=$\frac{2}{2��5}$=0.2 mol/��L•min��
�ʴ�Ϊ��0.2 mol/��L•min����
��3������ͬһ��Ӧ�С�ͬһʱ����ڣ������ʵķ�Ӧ����֮�ȵ��ڼ�����֮�ȣ�
����v��B����v��D��=0.2 mol/��L•min����0.2mol/��L•min��=2��n��n=2
�ʴ�Ϊ��2��
��4�����������ʶ������A�ķ�Ӧ���ʣ�
��v��A ��=5mol/�� L•min ��
����v�� B ��=6 mol/�� L•min ��֪��v��A ��=3mol/�� L•min ��
����v��C��=4.5mol/�� L•min ��֪��v��A ��=1.5 mol/�� L•min ��
����v��D ��=8mol/�� L•min ��֪��v��A ��=4mol/�� L•min ������÷�Ӧ�������ɴ�С��˳���ǣ�
�ʴ�Ϊ���٣��ܣ��ڣ��ۣ�
���� ���⿼���˻�ѧƽ������������Ӧ���ʡ�Ũ�ȵļ���Ӧ�ã����ջ����ǹؼ�����Ŀ�ϼ����4���ķ����ǣ����������ʶ������ͬһ���ʵķ�Ӧ���ʣ�Ȼ��Ƚϴ�С��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��2��4-���ױ� 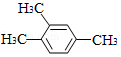 | B�� | 3-��-1-��ϩ | C�� | 2-��-1-���� 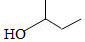 | D�� | 1��3-�������  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na��H2O�ķ�Ӧ�������ķ��ȷ�Ӧ���÷�Ӧ���Է����� | |
| B�� | �����£�NH4Cl��Һ��ˮϡ�ͣ�$\frac{c��N{H}_{3}•{H}_{2}O��•c��{H}^{+}��}{c��N{H}_{4}^{+}��}$���� | |
| C�� | 0.1 mol•L-1NaCN��Һ�к� HCN��CN-����ĿΪ0.1��6.02��1023 | |
| D�� | FeCl3��MnO2���ɼӿ�H2O2�ֽ⣬ͬ�������¶��߶�H2O2�ֽ����ʵĸı���ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | 1-�ȶ��� | C�� | �������� | D�� | �Ҵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ZnƬ��������CuƬ�Ǹ��� | B�� | ���������Ǵ�Zn�����·����Cu | ||
| C�� | ���Һ��PH���ֲ��� | D�� | CuƬ�������ݲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaHSO4��Һ��Ba��OH��2��Һ��Ӧ�����ԣ�2H++SO42-+Ba2++2OH-�TBaSO4��+2H2O | |
| B�� | ���ξ�ˮ��ԭ����Fe3++3H2O?Fe��OH��3�����壩+3H+ | |
| C�� | ��������ˮ���չ�ҵβ���е�SO2��2NH3•H2O+SO2�T2NH4++SO32-+H2O | |
| D�� | Fe2O3���ڹ����������Һ�У�Fe2O3+6H++2I-=2Fe2++I2+3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ij����������� | B�� | ʹ�ô��� | ||
| C�� | �����¶� | D�� | ����Ӧ��ϵ��ѹǿ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com