
(8分)(1)有三种有机物,其通式用CnH2nOn-2表示,当n依次为2,3,4时,其中能发生加聚反应获得常用高分子材料的是__________________(写结构简式,下同);水解后能生成乙酸和乙醇的是_______________;能被氢气还原为1一丙醇的是_________。
(2)1 mol含碳原子数为n mol的有机物完全燃烧,需O2 mol。
mol。
若该有机物4.4g与足量钠反应可收集560mL标准状况下 H2,该有机物分子结构中官能团名称是_____,若该有机物不能发生消去反应,其结构简式为________________。
(3)某有机物的式量是58,若是烃,则其结构简式可能是__________和____________;若是烃的含氧衍生物,且能发生银镜反应, 则反应的化学方程式是: ___________________________________。
(1)CH2=CH2 CH3COOCH2CH3 CH3CH2CHO(或丙烯醇);
(2)羟基,(CH3)3CCH2OH;(3)CH3CH2CH2CH3,CH3CH(CH3)2
CH3CH2CHO+2Ag(NH3)2OH 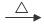 CH3CH2COONH4+2Ag+3NH3↑+H2O(或乙二醛的反应)
CH3CH2COONH4+2Ag+3NH3↑+H2O(或乙二醛的反应)
解析试题分析:(1)若n=2,该物质为C2H4,结构简式为CH2=CH2,发生加聚反应得到聚乙烯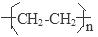 ;若n=4,则该物质的分子式为C4H8O2,其中CH3COOCH2CH3能发生水解反应得到CH3COOH和CH3CH2OH;若n="3," ,该物质为C3H6O,其中CH3CH2CHO能与氢气加成,被氢气还原为1一丙醇。(2)若该有机物4.4g与足量钠反应可收集560mL标准状况下 H2该有机物分子结构中官能团名称是羟基, 1 mol含碳原子数为n mol的有机物完全燃烧,需O2
;若n=4,则该物质的分子式为C4H8O2,其中CH3COOCH2CH3能发生水解反应得到CH3COOH和CH3CH2OH;若n="3," ,该物质为C3H6O,其中CH3CH2CHO能与氢气加成,被氢气还原为1一丙醇。(2)若该有机物4.4g与足量钠反应可收集560mL标准状况下 H2该有机物分子结构中官能团名称是羟基, 1 mol含碳原子数为n mol的有机物完全燃烧,需O2 mol。则该物质为饱和一元醇。n(OH)=2n(H2)=2×(0.56L÷22.4L/mol)=0.05mol.所以n(醇)= 0.05mol,M(醇)= 4.4g÷0.05mol=88g/mol。设去分子式为CnH2n+2O。14n+18=88.解得n=5.由于该有机物不能发生消去反应,则羟基连接的C原子的邻位C原子上没有H原子,所以该醇分子的结构简式为
mol。则该物质为饱和一元醇。n(OH)=2n(H2)=2×(0.56L÷22.4L/mol)=0.05mol.所以n(醇)= 0.05mol,M(醇)= 4.4g÷0.05mol=88g/mol。设去分子式为CnH2n+2O。14n+18=88.解得n=5.由于该有机物不能发生消去反应,则羟基连接的C原子的邻位C原子上没有H原子,所以该醇分子的结构简式为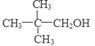 。(3)某有机物的式量是58,若是烃,假设为烷烃,分子式CnH2n+2,14n+2=58,解得n=4.则其结构简式可能是CH3CH2CH2CH3,CH3CH(CH3)2.若是烃的含氧衍生物,且能发生银镜反应,则该物质为醛。若为一元醛。设其分子式为CnH2nO。14n+16=58.解得n=3.结构简式为CH3CH2CHO。该物质反应的化学方程式是:CH3CH2CHO+2Ag(NH3)2OH
。(3)某有机物的式量是58,若是烃,假设为烷烃,分子式CnH2n+2,14n+2=58,解得n=4.则其结构简式可能是CH3CH2CH2CH3,CH3CH(CH3)2.若是烃的含氧衍生物,且能发生银镜反应,则该物质为醛。若为一元醛。设其分子式为CnH2nO。14n+16=58.解得n=3.结构简式为CH3CH2CHO。该物质反应的化学方程式是:CH3CH2CHO+2Ag(NH3)2OH  CH3CH2COONH4+2Ag+3NH3↑+H2O。也可能为OHC—CHO,方程式略。
CH3CH2COONH4+2Ag+3NH3↑+H2O。也可能为OHC—CHO,方程式略。
考点:考查物质的结构、性质、化学方程式书写及同式量的各类物质的性质的知识。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
写出下列反应的化学方程式
(1)乙烯和溴的四氯化碳溶液的反应_______________ ___________ 。
(2)乙醇与红热的铜丝反应得到乙醛 。
(3)乙酸乙酯与氢氧化钠反应_________________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
足球比赛中当运动员肌肉挫伤或扭伤时,队医会迅速对运动员的受伤部位喷射一种药剂——氯乙烷(沸点为12.27 ℃)进行局部冷冻麻醉应急处理。
(1)氯乙烷用于冷冻麻醉应急处理的原因是_______________________。
(2)制取CH3CH2Cl最好的方法是________。
| A.乙烷与氯气反应 | B.乙烯与氯气反应 | C.乙烷与HCl反应 | D.乙烯与HCl反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
实验室制取硝基苯的主要步骤如下:高考资源网
①配置一定比例的浓硫酸和浓硝酸的混合物,加入反应器
②向室温下的混合液中逐滴加入一定量的苯,充分振荡,混合均匀
③在50-60℃条件下发生反应,直到反应结束
④除去混合酸后,粗产品依次用蒸馏水和5﹪NaOH溶液洗涤,最后用蒸馏水洗涤
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏得到纯硝基苯
填写下列空白:
①配置一定比例的浓硫酸和浓硝酸的混合液时,操作注意事项是
②步骤③中,为了使反应在50-60℃下进行,常用的方法是 。
③步骤④中洗涤、分离粗硝基苯使用的仪器是 。
④步骤④中粗产品用5﹪NaOH溶液洗涤的目的是 。
⑤此反应可表示为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有机物X含有碳、氢、氧三种元素。
(1)探究X与钠反应产生气体的成分。
①X与钠反应产生的气体具有可燃性。将气体点燃,把一干燥的小烧杯罩在火焰上,片刻在烧杯壁上出现液滴,迅速倒转烧杯,向烧杯中加入少量澄清石灰水,未见浑浊。则X与钠反应产生的气体为________。
②根据苯、乙烷等碳氢化合物不能与钠反应产生上述气体这一事实,可得出X分子里有不同于烃分子里的氢原子存在。即有机物X除含有碳氢键之外,还有的化学键是________键。
(2)工业上, X可由乙烯与水反应制得,则X的分子式是________。
X分子含有的官能团的名称是________。写出X发生催化氧化反应的化学方程式______________。
X能被酸性高锰酸钾或重铬酸钾氧化为生活中的另一种重要的有机化合物Y,X与Y发生反应的化学方程式是________________。为了提高该反应的反应速率,可采取的措施是_______________。可用某溶液除去产品中混有的杂质,写出除杂过程发生反应的化学反应方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(6分)某链烃3.6g和Cl2发生取代反应,控制反应条件使其仅生成一氯代物,将反应生成的气体(一氯代物为液体)用NaOH溶液吸收恰好和0.1mol·L-1 NaOH溶液500mL完全反应,试解答下列问题:
(1)求该烃的相对分子质量;
(2)若该烃既不能使酸性KMnO4溶液褪色,又不能使溴水褪色,试求该烃的分子式。
(3)若该烃的一氯代物只有一种,试确定该烃的结构简式 (要求写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
电石中的碳化钙和水能完全反应: CaC2+2H2O=C2H2↑+Ca(OH)2,使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量。
(1)若用下列仪器和导管组装实验装置:
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是:( )接( )接( )接( )接( )接( )。
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞。
②检查装置的气密性。
③在仪器6和5中注入适量水。
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计)。
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不发生气体时,关闭活塞。
正确的操作顺序(用操作编号填写)是 。
(3)若实验产生的气体有难闻的臭鸡蛋这是因为含有 杂质。检验此杂质的反应为 。
(4)若实验时称取的电石1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数是 %。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
将下图所列仪器组装成一套实验室蒸馏石油的装置,并进行蒸馏得到汽油和煤油。
(1)上图中A、B、C三种仪器的名称分别是 ; ; 。
(2)将以上仪器(一)→(六),按连接顺序表示(用字母a,b,c……表示):
e接i; 接 ;k接l; 接 ; 接 。
(3)A仪器中,c口是 ,d口是 。
(4)蒸馏时,温度计水银球应在 位置。
(5)在B中注入原油后,再加几片碎瓷片的目的是 。
(6)给B加热,收集到沸点在60~150 ℃之间的馏分是 ,收集到150~300 ℃之间的馏分是 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某有机物的结构为 , ,下列有关说法正确的是
, ,下列有关说法正确的是
| A.1 mol该物质与足量淮溴水反应,最多消耗2 molBr2 |
| B.1mol该物质最多能与2mol NaOH反应 |
| C.l mol该物质晟多能与3 mol H2加成 |
| D.该物质的核磁共振氢谱共有6个吸收峰 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com