
| 元素A | 元素B | 元素C | 元素X | 元素Y | 元素Z |
| 单质是一种常见金属,与元素X形成黑色和砖红色两种化合物 | 单质是一种黄绿色气体 | 短周期中金属性最强,与X反应能生成两种化合物 | 最外层电子数是内层电子数的3倍,能形成双原子阴离子 | 单质为双原子分子,结构中σ键与π键数目比为1:2 | 阳离子就是一个质子 |
| 1mol |
| 100L |


科目:高中化学 来源: 题型:
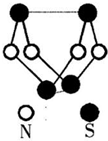 (2010?合肥三模)现代无机化学对硫一氮化合物的研究是最为活跃的领域之一.其中图是已经合成的最著名的硫一氮化合物的分子结构.下列说法错误的是( )
(2010?合肥三模)现代无机化学对硫一氮化合物的研究是最为活跃的领域之一.其中图是已经合成的最著名的硫一氮化合物的分子结构.下列说法错误的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
(2010?合肥三模)如图所示,利用培养皿进行实验.实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面. 下表中对实验现象所做的解释不正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 (2010?合肥三模)在一密闭容器中充入4mol SO2和一定量O2,发生反应:2SO2(g)+O2(g)?2SO3(g)△H=一196.6kJ?mol-1.则下列说法正确的是( )
(2010?合肥三模)在一密闭容器中充入4mol SO2和一定量O2,发生反应:2SO2(g)+O2(g)?2SO3(g)△H=一196.6kJ?mol-1.则下列说法正确的是( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com