
【题目】同温同压下,质量相同的O2、CO、CH4三种气体,下列说法错误的是
A. 所占的体积由大到小的顺序是:CH4>CO >O2
B. 所含的电子数由多到少是:CH4>CO>O2
C. 所含原子数由多到少的顺序是:CH4>CO >O2
D. 密度由大到小的顺序是:O2>CO>CH4
【答案】B
【解析】A、根据n=![]() 可知,质量相同时,摩尔质量越大,物质的量越小,则同温同压下体积与物质的量成正比,质量相同的CO、O2、CH4三种气体,所占的体积由大到小的顺序是:CH4>CO>O2,选项A正确;B、取mg三种气体,质量相同的CO、O2、CH4三种气体含电子数分别为:
可知,质量相同时,摩尔质量越大,物质的量越小,则同温同压下体积与物质的量成正比,质量相同的CO、O2、CH4三种气体,所占的体积由大到小的顺序是:CH4>CO>O2,选项A正确;B、取mg三种气体,质量相同的CO、O2、CH4三种气体含电子数分别为: ![]() ×14,
×14, ![]() ×16,
×16, ![]() ×10,所含的电子数由多到少是:CH4>CO=O2,选项B错误;C、根据n=
×10,所含的电子数由多到少是:CH4>CO=O2,选项B错误;C、根据n=![]() 可知,质量相同时,摩尔质量越大,物质的量越小,分子数越少,同温同压下,质量相同的CO、O2、CH4,分子数由多到少的顺序是:CH4>CO>O2,选项C正确;D、同温同压下,密度之比等于摩尔质量之比,CO、O2、CH4三种气体摩尔质量由大到小的顺序是: O2>CO>CH4,密度之比为: O2>CO>CH4,选项D正确。答案B。
可知,质量相同时,摩尔质量越大,物质的量越小,分子数越少,同温同压下,质量相同的CO、O2、CH4,分子数由多到少的顺序是:CH4>CO>O2,选项C正确;D、同温同压下,密度之比等于摩尔质量之比,CO、O2、CH4三种气体摩尔质量由大到小的顺序是: O2>CO>CH4,密度之比为: O2>CO>CH4,选项D正确。答案B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A. 14 g乙烯和丙烯混合气体中的氢原子数为2NA
B. 1 mol N2与4 mol H2反应生成的NH3分子数为2NA
C. 1 mol Fe溶于过量硝酸,电子转移数为2NA
D. 标准状况下,2.24 L CCl4含有的共价键数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 X、Y、Z、W四种物质在一定条件下具有如图所示的转化关系,下列判断正确的是
![]()
A.若图中反应均为非氧化还原反应,当W为一元强碱时,则X可能是NaAlO2
B.若图中反应均为非氧化还原反应,当W为一元强酸时,则X可能是NH3
C.若图中反应均为氧化还原反应,当W为非金属单质时,则Z可能是CO2
D.若图中反应均为氧化还原反应,当W为金属单质时,则Z可能是FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)① ![]() 的系统命名:_______________。
的系统命名:_______________。
②CH3CH2CHO的银镜反应的化学方程式:_____________________。
(2)有机物A的结构简式为![]() ,它可通过不同化学反应分别制得B、C、D和E 四种物质。
,它可通过不同化学反应分别制得B、C、D和E 四种物质。
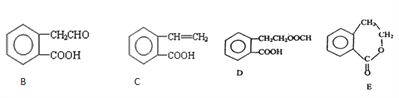
请回答下列问题:
(1)指出反应的类型:A→C:_______________ 。
(2)在A~E五种物质中,互为同分异构体的是_______________(填代号)。
③己知HCHO分子中所有原子都在同一平面内,则在上述分子中所有的原子有可能都在同一平面的物质是____________(填代号)。
④ C能形成高聚物.该高聚物的结构简式为:__________________。
⑤ 写出D与NaOH溶液共热反应的化学方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某品牌饮用矿泉水的标签的部分内容如下。下列说法正确的是
饮用矿物质水
净含量:500 mL 配料表:纯净水 硫酸镁 氯化钾 保质期:12 个月
主要离子成分: 钾离子(K+):1.0~27.3 mg/L 镁离子(Mg2+):0.1~4.8 mg/L
A. 标签上的离子的浓度是物质的量浓度
B. 该品牌饮用矿泉水中c(Mg2+)最大值为 2×10—4 mol/L
C. 取少量待测液加入稀盐酸酸化,再滴入硝酸银,出现白色沉淀,说明有氯离子
D. 一瓶该品牌饮用矿泉水中 SO42-的物质的量不超过 1×10—5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。

(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式:___________________。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇的氧化反应是________反应。
(2)甲和乙两个水浴作用不相同。甲的作用是________;乙的作用是________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有________。要除去该物质,可先在混合液中加入________(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过________(填实验操作名称)即可除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 1 mol 金刚石晶体中,平均含有1 mol C—C键
B. BCl3中B原子以sp2杂化,分子为平面三角形
C. 氢键具有方向性和饱和性,也属于一种化学键
D. (HO)2RO3的酸性比(HO)2RO2弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
化合物G是治疗高血压的药物“比索洛尔”的中间体,一种合成G的路线如下:

已知以下信息:
①A的核磁共振氢谱为单峰;B的核磁共振氢谱为三组峰,峰面积比为6∶1∶1。
②D的苯环上仅有两种不同化学环境的氢;1molD可与1mol NaOH或2mol Na反应。
回答下列问题:
(1)A的结构简式为____________。
(2)B的化学名称为____________。
(3)C与D反应生成E的化学方程式为____________。
(4)由E生成F的反应类型为____________。
(5)G是分子式为____________。
(6)L是D的同分异构体,可与FeCl3溶液发生显色反应,1mol的L可与2mol的Na2CO3反应,L共有______种;其中核磁共振氢谱为四组峰,峰面积比为3∶2∶2∶1的结构简式为___________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中D原子的质子数是其M层电子数的三倍,下列说法不正确的是 ( )

A. A有5种正价,与B可形成6种化合物
B. 工业上常通过电解熔融态C2B3的方法来获得C的单质
C. 简单离子的半径由大到小为:E>A>B>C
D. D、E两元素形成的化合物每种原子最外层都达到了8e-稳定结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com