
【题目】某温度,在1L恒容密闭容器中,加入10molCO、7molH2S,发生如下反应:CO(g)+H2S(g)COS(g)+H2(g),达平衡时CO物质的量为8mol,下列说法正确的是( )
A.该温度下,化学平衡常数K=0.1
B.H2S的平衡转化率为20%
C.增大CO浓度,平衡正向移动,可以提高CO的转化率
D.升高温度,H2S浓度增加,表明该反应正方向是吸热反应
【答案】A
【解析】解:在1L恒容密闭容器中,加入10molCO、7molH2S,发生如下反应:CO(g)+H2S(g)COS(g)+H2(g),达平衡时CO物质的量为8mol,说明反应转化了2molCO,则
CO(g) | + | H2S(g) | COS(g) | + | H2(g) | ||
起始(mol) | 10 | 7 | 0 | 0 | |||
转化(mol) | 2 | 2 | 2 | 2 | |||
平衡(mol) | 8 | 5 | 2 | 2 |
A.因体积为1L,则浓度与物质的量数值相等,该温度下,化学平衡常数K= ![]() =0.1,故A正确;
=0.1,故A正确;
B.H2S的平衡转化率为 ![]() ×100%=28.6%,故B错误;
×100%=28.6%,故B错误;
C.增大CO浓度,平衡正向移动,但CO的转化率反而降低,故C错误;
D.升高温度,H2S浓度增加,说明平衡逆向移动,表明该反应逆方向是吸热反应,则正反应为放热反应,故D错误.
故选A.
【考点精析】解答此题的关键在于理解化学平衡的计算的相关知识,掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


科目:高中化学 来源: 题型:
【题目】如图所示,a、b、c、d、e为元素周期表中前4周期的一部分元素,下列有关叙述正确的是( )
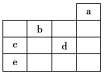
A. 元素b位于第ⅥA族,有+6、-2价两种常见化合价
B. 五种元素中,元素e的性质最稳定
C. 元素c和d的最高价氧化物对应的水化物的酸性:c>d
D. 元素c和e的气态氢化物的稳定性:c>e
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种食用香料,主要用于奶油、酸奶的加工.它也可用于有机合成,以A为原料制备阴离子树脂M和新型高分子材料N的合成路线如下: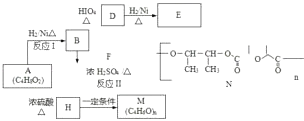
已知: ![]()
(1)写出反应类型:反应I;反应II .
(2)A中官能团的名称是;A属于酯类的同分异构体有种,其中只含一个甲基的同分异构的结构简式是: .
(3)D与新制Cu(OH)2反应的化学方程式是 .
(4)M的结构简式为 .
(5)某有机物CxHyOz(0<z<5)与A以任意比混合后燃烧,每摩尔混合物消耗5摩尔氧气.请写出该有机物可能的分子式 . (写两种)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为常见温室气体,B为淡黄色氧化物,C为常见液体,D为黄绿色气体单质,相互反应的关系如右图所示,M的水溶液能杀菌消毒。下列有关叙述正确的是
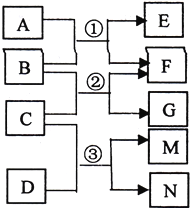
A. 4.4gA含有4.4NA个质子
B. 7.8gB与足量A发生反应①,共转移0.2NA电子
C. 反应③的离子方程式为:Cl2+H2O![]() 2H++Cl-+ ClO-
2H++Cl-+ ClO-
D. M的电子式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.植物油氢化过程发生了加成反应B.淀粉和纤维素互为同分异构体
C.环己醚与苯可用酸性KMnO4溶液鉴别D.水可以用来分离溴苯和苯的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】混合气体由N2和CH4组成,测得混合气体在标准状况下的密度是0.821g/L,则混合气体中N2和CH4的体积之比为( )
A. 5∶1 B. 4∶1 C. 1∶4 D. 1∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中错误的是 ( )
A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
C.蒸发结晶时应将溶液蒸干
D.称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com