
向50 mL稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如下图所示,且每一段只对应一个反应。下列说法正确的是( )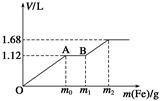
| A.开始时产生的气体为H2 |
| B.AB段产生的反应为置换反应 |
| C.所用混合溶液中c(HNO3)=0.5 mol·L-1 |
| D.参加反应铁粉的总质量m2=5.6 g |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
下列各组反应中,硝酸既表现了氧化性,又表现了酸性的是
| A.C+HNO3 | B.SO2+HNO3 | C.Fe(OH)3+HNO3 | D.FeO+HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
a mol FeS与b mol Fe3O4投入到V L c mol·L-1的硝酸溶液中恰好完全反应,假设只产生NO气体。所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的硝酸为
| A.(a+3b) mol |
B.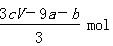 |
C.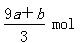 |
| D.(cV-3a-9b) mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
a mol FeS与b mol FeO投入到V L、c mol/L的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )
①(a+b)×63 g ②(a+b)×189 g ③(a+b)mol ④[Vc-(9a+b)/3]mol
| A.①④ | B.②③ | C.①③ | D.②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示。有关说法不正确的是( )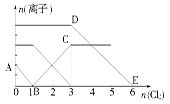
| A.线段BC代表Fe3+物质的量的变化情况 |
| B.原混合溶液中c(FeBr2)=6 mol/L |
| C.当通入Cl2 2 mol时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| D.原溶液中n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氯酸是一种强酸,浓度超过40%时会发生分解,该反应可表示为aHClO3―→bO2↑+cCl2↑+dHClO4+eH2O,下列有关说法不正确的是( )
| A.由反应可确定氧化性:HClO3>O2 |
| B.由非金属性:Cl>S,可推知酸性:HClO3>H2SO4 |
| C.若氯酸分解所得1 mol混合气体的质量为45 g,则反应方程式可表示为3HClO3=2O2↑+Cl2↑+HClO4+H2O |
| D.若化学计量数a=8,b=3,则生成3 mol O2时该反应转移20 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据下列事实:①A+B2+=A2++B;②D+2H2O=D(OH)2+H2↑;③以B、E为电极与E的盐溶液组成原电池,电极反应为E2++2e-=E,B-2e-=B2+。由此可知A2+、B2+、D2+、E2+的氧化性强弱关系是( )。
A.D2+>A2+>B2+>E2+
B.A2+>B2+>D2+>E2+
C.D2+>E2+>A2+>B2+
D.E2+>B2+>A2+>D2+
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
为实现中国消除碘缺乏病的目标,卫生部规定食盐必须加碘,其中碘以碘酸钾(KIO3)形式存在,已知在溶液中I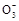 可和I-发生反应:I
可和I-发生反应:I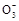 +5I-+6H+
+5I-+6H+ 3I2+3H2O,根据此反应,可用试纸和一些生活中常见物质进行实验,证明食盐中存在I
3I2+3H2O,根据此反应,可用试纸和一些生活中常见物质进行实验,证明食盐中存在I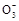 ,可供选用的物质有:①自来水②蓝色石蕊试纸,③碘化钾淀粉试纸④淀粉⑤食糖⑥食醋⑦白酒。进行上述实验时必须使用的物质是( )。
,可供选用的物质有:①自来水②蓝色石蕊试纸,③碘化钾淀粉试纸④淀粉⑤食糖⑥食醋⑦白酒。进行上述实验时必须使用的物质是( )。
| A.①③ | B.③⑥ | C.②④⑥ | D.①②④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某溶液中含有的溶质是FeBr2、FeI2,若先向该溶液中通入一定量的氯气,再向反应后的溶液中滴加KSCN溶液,溶液变为红色,则下列叙述正确的是 ( )。
①原溶液中的Br-一定被氧化;②通入氯气之后原溶液中的Fe2+一定有部分或全部被氧化;③不能确定通入氯气后的溶液中是否存在Fe2+;④若取少量所得溶液,再加入CCl4,静置、分液,向上层溶液中加入足量的AgNO3溶液,只产生白色沉淀,说明原溶液中的I-、Fe2+、Br-均被完全氧化。
| A.①②③ | B.②③④ | C.①③④ | D.①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com