
【题目】用①H2O ②H2O2 ③Ba(OH)2 ④Na2O2 ⑤MgCl2 ⑥Ar ⑦CO2 ⑧CaF2 ⑨NH4Cl ⑩CaO2 ![]() Ca(ClO)2
Ca(ClO)2 ![]() N2H4等物质填空。
N2H4等物质填空。
(1)只存在离子键的是________;
(2)由离子键和极性键构成的是_________;
(3)由离子键和非极性键构成的是_________;
(4)由极性键和非极性键构成的是_________;
(5)写出下列物质的电子式:Na2S2:_________;(NH4)2S:______。
【答案】 ⑤⑧ ③⑨ ④⑩ ② 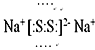
![]()
【解析】①H2O属于共价化合物,只存在极性共价键;②H2O2属于共价化合物,存在极性共价键和非极性共价键;③Ba(OH)2属于离子化合物,存在离子键和极性共价键;④Na2O2属于离子化合物,存在离子键和非极性共价键;⑤MgCl2属于离子化合物,只存在离子键;⑥Ar是单原子分子,不存在化学键;⑦CO2属于共价化合物,存在极性共价键;⑧CaF2属于离子化合物,只存在离子键;⑨NH4Cl属于离子化合物,存在离子键和极性共价键;⑩CaO2属于离子化合物,存在离子键和非极性共价键; ![]() Ca(ClO)2属于离子化合物,存在离子键和极性共价键;
Ca(ClO)2属于离子化合物,存在离子键和极性共价键; ![]() N2H4属于共价化合物,存在极性共价键和非极性共价键。
N2H4属于共价化合物,存在极性共价键和非极性共价键。
(1)只存在离子键的是⑤⑧,故答案为:⑤⑧;
(2) 由离子键和极性键构成的是③⑨,故答案为:③⑨;
(3)由离子键和非极性键构成的是④⑩,故答案为:④⑩;
(4) 由极性键和非极性键构成的是②,故答案为:②;
(5) Na2S2的电子式为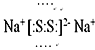 ;(NH4)2S的电子式为
;(NH4)2S的电子式为![]() ,故答案为:
,故答案为: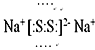 ;
;![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A. 聚氯乙烯分子中含有碳碳双键
B. 戊烷有5种同分异构体
C. 以淀粉为原料可以制备乙酸乙酯
D. 油脂的皂化反应属于加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中盛有4molNa2O2与3molNaHCO3,将其加热到150℃,经充分反应后,剩余的固体物质是( )
A. 1mol Na2CO3和3molNaOH
B. 2mol Na2CO3和1molNa2O2
C. 3mol Na2CO3和3molNaOH 和1molNa2O2
D. 1mol Na2CO3和2molNaOH 和3molNa2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾由多种污染物形成,其中包含颗粒物(包括PM2.5在内)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用。回答下列问题:
(1)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol -1
2SO3(g) ΔH=-196.6 kJ·mol -1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g) 的ΔH= kJ·mol-1。
SO3(g)+NO(g) 的ΔH= kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于恒温恒容的密闭容器中发生上述反应,下列能说反应达到平衡状态的有 。(填字母)
a.体系密度保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1:5,则平衡常数K= 。
(2)CO可用于合成甲醇,反应的化学方程式为 CO(g)+2H2(g)![]() CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。

(3)一种用NH3脱除烟气中NO的原理如下图:

①该脱硝原理中,NO最终转化为H2O和 (填化学式)。
②当消耗1 mol NH3和0.5 molO2时,除去的NO在标准状况下的体积为 。
(4)NO直接催化分解(生成N2和O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40℃下分解生成两种化合物,反应物与生成物三者的物质的量之比比3:1:1,则该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以惰性电极电解足量的CuSO4溶液。若阳极上产生气体的物质的量为0.0100 mol,则阴极上析出铜的质量为( )
A. 0.64 g B. 1.28 g C. 2.56 g D. 5.12 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g。向另—份中逐渐加入铁粉,产生气体的量随铁粉质量的增加的变化关系如图所示(已知硝酸只被还原为 NO气体)。下列分析或结果错误的是

A. 原混合酸中NO3-的物质的量为0.1mol
B. 第二份溶液中最终溶质为FeSO4
C. OA段产生的是NO,AB段的反应为Fe+2Fe3+==3Fe2+,BC段产生氢气
D. H2SO4浓度为2.5 molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用下图所示装置制备气体(酒精灯可以根据需要选择),对应说法正确的是

选项 | ①中药品 | ②中药品 | ③中药品 | ④中药品 | 制备气体 | ⑥中药品及作用 |
A | 浓盐酸 | MnO2 | 饱和食盐水 | 浓硫酸 | C12 | NaOH溶液,尾气吸收 |
B | 稀硝酸 | Cu | 烧碱溶液 | 浓硫酸 | NO | Na()H溶液,尾气吸收 |
C | 浓盐酸 | 大理石 | 饱和Na2CO3溶液 | 浓硫酸 | CO2 | 澄清石灰水,检验CO2 |
D | 浓盐酸 | Zn | 水 | 浓硫酸 | H2 | 可撤去 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com