
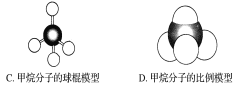
【题目】Ⅰ.如图所示是几种烷烃的球棍模型,试回答下列问题:

(1)A、B、C三者的关系是___。
(2)A的分子式为___,C的名称为__。
(3)写出C的同分异构体的结构简式:___。
Ⅱ.如图均能表示甲烷的分子结构,其中更能反映其真实的存在状况的是__(填字母)。

【答案】同系物 C2H6 正丁烷 (CH3)2CHCH3 D
【解析】
烷烃由C和H元素组成,大球表示C,小球表示H,其通式为CnH2n+2,所以A、B、C的结构简式为CH3CH3、CH3CH2CH3、CH3CH2CH2CH3。
(1)三者的关系为碳原子数不同的烷烃,应属同系物,故答案为:同系物;
(2)根据图示可知,A的分子式为:C2H6,C的名称为正丁烷,故答案为:C2H6,正丁烷;
(3)丁烷的同分异构体为异丁烷,其结构简式为:(CH3)2CHCH3,故答案为:(CH3)2CHCH3;
Ⅱ.由于比例模型表示的是原子的相对大小及连接形式,更接近分子的真实结构,所以D正确,故答案为:D。


科目:高中化学 来源: 题型:
【题目】在 2L 密闭容器中,3mol A 和 1molB 发生反应:3A(g)+B(g)2C(g)+2D(g),10s 末时,生成 1.2mol C,下列说法正确的是
A.10s 内,v(D)=0.12 mol/(L·s)B.10s 末时,物质 A 的转化率为 60%
C.10s 末时,B的浓度为0.3mol/LD.10s 末时,C 的物质的量分数为 15%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】200℃、101kPa时,在密闭容器中充入1molH2和1molI2,发生反应I2(g)+H2(g)![]() 2HI(g) ΔH=-14.9 kJ/mol。反应一段时间后,能说明反应已经达到化学平衡状态的是
2HI(g) ΔH=-14.9 kJ/mol。反应一段时间后,能说明反应已经达到化学平衡状态的是
A. 放出的热量小于14.9 kJ
B. 反应容器内压强不再变化
C. HI生成的速率与HI分解的速率相等
D. 单位时间内消耗a mol H2,同时生成2a mol HI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2、漂白液(有效成分为 NaClO)在生产、生活中广泛用于杀菌、消毒。
(1)电解 NaCl 溶液生成Cl2的化学方程式是________________。
(2)Cl2溶于H2O、NaOH 溶液即获得氯水、漂白液。
①干燥的氯气不能漂白物质,但氯水却有漂白作用,说明起漂白作用的物质是_____。
②25℃,Cl2与H2O、NaOH 的反应如下:
反应Ⅰ | Cl2+H2O |
反应Ⅱ | Cl2+2OH- |
解释不直接使用氯水而使用漂白液做消毒剂的原因_____。
(3)家庭使用漂白液时,不宜直接接触铁制品,漂白液腐蚀铁的电极反应为:Fe-2e-=Fe2+;ClO-发生的电极反应式为____________。
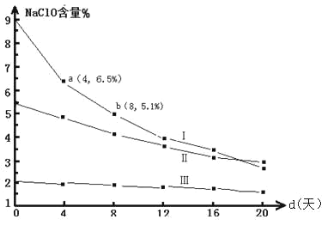
(4)研究漂白液的稳定性对其生产和保存有实际意义。30℃时,pH=11 的漂白液中NaClO 的质量百分含量随时间变化如下:
比较分解速率 v(I)、 v(II)的大小关系_____,原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各反应达到化学平衡,加压或降温都能使化学平衡向逆反应方向移动的是
A. 2NO2![]() N2O4(正反应为放热反应) B. C(s)+CO2
N2O4(正反应为放热反应) B. C(s)+CO2![]() 2CO(正反应为吸热反应)
2CO(正反应为吸热反应)
C. N2+3H2![]() 2NH3(正反应为放热反应) D. H2S
2NH3(正反应为放热反应) D. H2S![]() H2+S(s)(正反应为吸热反应)
H2+S(s)(正反应为吸热反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,所设计的装置如图所示:
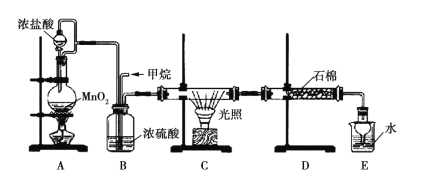
(1)A中制取Cl2的反应的化学方程式是_________________________。
(2)B装置的作用:①______;②______;③______。
(3)D装置中的石棉上吸附着潮湿的KI,其作用是________________。
(4)E装置的作用是_____(填序号)。
A.收集气体 B.吸收氯气 C.吸收氯化氢
(5)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法是______________。
(6)将1 mol CH4与Cl2发生取代反应,测得4种有机取代产物的物质的量相等,则消耗的氯气的物质的量是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是应用最广泛的金属,铁的卤化物,氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)铁元素在周期表中的位置为_______。
(2)要确定铁的某氯化物FeClx的化学式,可利用离子交换和滴定的方法。实验中称取0.54 g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40 mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0 mL。则x=_____。
(3)实验室用铁氰化钾确定某铁的氯化物中是否含有FeCl2,该反应的离子方程式为_____。
(4)Fe(OH)3固体与氢碘酸反应时可生成棕色物质的离子方程式为________。
(5)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为_______。
(6)实验室准确称取1.44g草酸亚铁固体,在空气中灼烧,得到0.773g铁的氧化物,写出该铁的氧化物的化学式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,铝土矿![]() 含有
含有![]() 、FeO、
、FeO、![]() 、
、![]() 等物质
等物质![]() 用硫酸浸。下列说法中错误的是
用硫酸浸。下列说法中错误的是![]()
![]()
A.向浸出后的溶液加入过量NaOH溶液后存在:![]() 、
、![]() 、
、![]() 、
、![]()
B.向浸出后的溶液加入过量氨水后存在:![]() 、
、![]() 、
、![]() 、
、![]()
C.向浸出后的溶液通入过量HI后存在:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]()
D.若铝土矿改用NaOH溶液浸,浸出后的溶液中存在:![]() 、
、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由乙烷和乙烯都能制得一氯乙烷。
(1)由乙烷制一氯乙烷的化学方程式为____________,反应类型为______________。
(2)在催化剂作用下,由乙烯制一氯乙烷的化学方程式为____________,反应类型为______________。
(3)以上两种方法中_________[填“(1)”或“(2)”]更适合用来制取一氯乙烷,原因是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com