
【题目】2 mol O2和________g CH4在标准状况下占有相同的体积,其体积为________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某实验小组学生用50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量计算反应热。下列说法正确的是( )
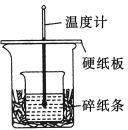
A.如图条件下实验过程中没有热量损失
B.图中实验装置缺少环形玻璃搅拌棒
C.烧杯间填碎纸条的主要作用是固定小烧杯
D.若改用60 mL 0.50 mol/L盐酸跟50 mL 0.55 mol/L的NaOH溶液进行反应,从理论上说所求放出热量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50molL﹣1盐酸与50mL0.55molL﹣1 NaOH溶液在如下图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器的名称是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)。
(4)如果用60mL 0.50molL﹣1盐酸与50mL 0.55molL﹣1 NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向50mL 0.018molL﹣1的AgNO3溶液中加入50mL 0.02molL﹣1的盐酸生成沉淀.已知Ksp(AgCl)=1.8×10﹣10 , 则生成沉淀后的溶液中c(Ag+)与pH分别为( )
A.1.8×10﹣7 molL﹣1 , 2
B.1×10﹣7 molL﹣1 , 2
C.1.8×10﹣7 molL﹣1 , 3
D.1×10﹣7 molL﹣1 , 3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往100 mL 1 mol·L -1 的AlCl3 溶液中滴加1 mol·L -1 的NaOH溶液,得3.9 g沉淀,则加入NaOH溶液的体积可能是
A. 100 mL B. 200 mL C. 300 mL D. 350 mL
【答案】D
【解析】氯化铝的物质的量是0.1mol,生成的氢氧化铝是3.9g÷78g/mol=0.05mol,如果氯化铝过量,则根据Al3++3OH-===Al(OH)3↓可知需要氢氧化钠是0.15mol,溶液体积是0.15mol÷1mol/L=0.15L=150mL;如果氢氧化钠过量,生成的氢氧化铝部分溶解,则0.1mol氯化铝需要0.3mol氢氧化钠生成0.1mol氢氧化铝,其中有0.05mol氢氧化铝溶解,根据Al(OH)3+OH-===AlO2-+2H2O可知又需要0.05mol氢氧化钠,则溶液体积是0.35mol÷1mol/L=0.35L=350mL,答案选D。
点睛:该题也可以借助图像解答,例如把强碱溶液逐滴加入到铝盐(Al3+)溶液中至过量的现象是:先有白色沉淀产生,然后沉淀逐渐溶解,有关反应:A→B:Al3++3OH-===Al(OH)3↓、B→D:Al(OH)3+OH-===AlO2-+2H2O,图像: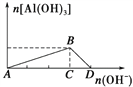 ,作纵坐标的垂线与图像有2个交点(B点除外),因此需要氢氧化钠的物质的量也有两种情况,解答时可以灵活应用。
,作纵坐标的垂线与图像有2个交点(B点除外),因此需要氢氧化钠的物质的量也有两种情况,解答时可以灵活应用。
【题型】单选题
【结束】
11
【题目】某溶液中有Fe3+、Mg2+ 、Fe2+ 和Al3+ 四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量增加的阳离子是
A. Fe3+ B. Mg2+ C. Fe2+ D. Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.非金属元素形成的化合物不可能是离子化合物
B.金属原子和非金属原子间也可形成共价键
C.离子化合物中可能含有共价键
D.共价化合物中不能含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用下列装置模拟工业生产制备少量硝酸. 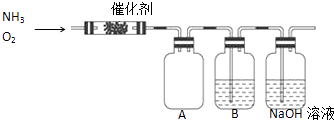
(1)B中试剂为 , NaOH溶液的作用是 .
(2)用过氧化钠与水反应制备氧气的化学方程式为 .
(3)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上.下列图示中,能够正确表示该反应过程能量变化的是 .
A.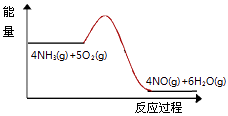
B.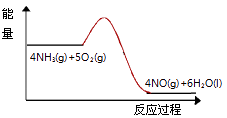
C.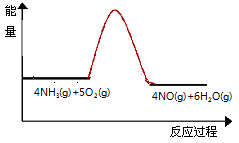
D.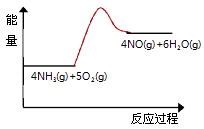
(4)已知2NO2(g)2NO(g)+O2(g)△H
NO2(g) ![]() N(g)+2O(g)
N(g)+2O(g)
NO(g) ![]() N(g)+O(g)
N(g)+O(g)
O2(g) ![]() 2O(g)
2O(g)
①计算反应的△H= .
②请解释高温下,氨气与氧气反应难以生成NO2的原因 .
(5)控制氨气和氧气的比例是制备硝酸的关键.
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟.请用化学方程式表示白烟产生的原因 .
②欲使氨气尽可能完全转化为硝酸,理论上n(NH3):n(O2)的最佳比例为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是用98%的浓H2SO4(ρ=1.84 g·cm-3;物质的量浓度为18.4mol/L)配制0.5 mol·L-1的稀硫酸500 mL的实验操作,请按要求填空:
(1)所需浓硫酸的体积为________。
(2)如果实验室有10 mL、20 mL、50 mL的量筒,应选________的最好,量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将(填“偏高”、“偏低”或“无影响”)____________。
(3)将量取的浓硫酸沿烧杯内壁慢慢注入盛有约100 mL水的烧杯中,并不断搅拌,目
的是________________________。
(4)将冷却至室温的上述溶液沿________注入________中,并用50 mL蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液要转入到容量瓶中,并振荡。
(5)加水至距刻度线1 cm~2 cm处,改用________加水至刻度线,使溶液的________正好跟刻度线相平,把容量瓶塞好,反复颠倒振荡,摇匀溶液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com