
| A. | 18.4mol•L-1 34.7% | B. | 20.4mol•L-1 38.5% | ||
| C. | 18.4mol•L-1 38.5% | D. | 20.4mol•L-1 34.7% |
分析 NH3溶于水后虽然大部分生成NH3•H2O,但在计算时,仍以NH3作为氨水中的溶质,设水的体积为1L,则氨气的体积为700L,根据n=$\frac{m}{M}$计算氨气的物质的量,再根据m=nM计算氨气质量,溶液质量=氨气质量+水的质量,进而计算溶液质量分数,根据V=$\frac{m}{ρ}$计算溶液体积,再根据c=$\frac{n}{V}$计算溶液物质的量浓度.
解答 解:NH3溶于水后虽然大部分生成NH3•H2O,但在计算时,仍以NH3作为氨水中的溶质,
设水的体积为1L,氨气的体积为700L,则氨气的物质的量为:$\frac{700mL}{22.4L/mol}$=31.25mol,
溶液的质量为1000g+31.25mol×17g/mol=1531.25g,
溶液的体积为:$\frac{1531.25g}{900g/L}$=1.7L,
则氨水的质量分数为:$\frac{31.25mol×17g/mol}{1531.25g}$×100%=34.7%;
氨水的物质的量浓度为:c=$\frac{31.25mol}{1.7L}$=18.4 mol/L,
故选A.
点评 本题考查物质的量浓度和质量分数的计算,难度中等,溶液的体积计算是解答本题的关键也是易错点,注意掌握物质的量浓度、溶质质量分数的概念及表达式,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:实验题
 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
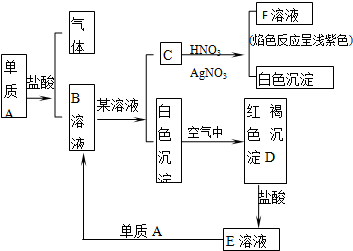
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4个--CH3,能生成4种一氯代物 | B. | 3个--CH3,能生成4种一氯代物 | ||
| C. | 3个--CH3,能生成5种一氯代物 | D. | 2个--CH3,能生成4种一氯代物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合物$\stackrel{加水}{→}$溶液$→_{足量}^{K_{2}SO_{4}溶液}$$\stackrel{蒸发结晶}{→}$KNO3固体 | |
| B. | 混合物$\stackrel{加水}{→}$溶液$→_{足量}^{K_{2}CO_{3}溶液}$$\stackrel{过滤}{→}$滤液$\stackrel{蒸发结晶}{→}$KNO3固体 | |
| C. | 混合物$\stackrel{加水}{→}$溶液$→_{足量}^{K_{2}CO_{3}溶液}$$\stackrel{过滤}{→}$滤液$→_{足量}^{HNO_{3}溶液}$$\stackrel{蒸发结晶}{→}$KNO3固体 | |
| D. | 混合物$\stackrel{加水}{→}$溶液$→_{足量}^{K_{2}SO_{4}溶液}$$\stackrel{过滤}{→}$滤液$→_{足量}^{HNO_{3}溶液}$$\stackrel{蒸发结晶}{→}$KNO3固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 农村推广建造沼气池,实现了生物质能向热能的转化 | |
| B. | 光-生物质能转换的本质是光-化学能的转换 | |
| C. | 科学家们预言,氢能将成为21世纪的重要能源 | |
| D. | 化石燃料蕴藏的能量来自远古时期生物体所吸收利用的太阳能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com