
【题目】A、E为短周期元素的单质,B、C为化合物,它们之间的转化关系如图所示:
A ![]() B
B ![]() C
C
请写出全部可能的情况.(写化学式,可不填满,也可补充)
第一种情况:A、B、C .
第二种情况:A、B、C .
第三种情况:A、B、C .
第四种情况:A、B、C .
…
【答案】C;CO;CO2;S;SO2;SO3;N2;NO;NO2;Na;Na2O;Na2O2;
【解析】解:A、E为短周期元素中的某单质,B、C为其化合物,能连续与E反应,E为O2 , 则B、C应为氧化物,短周期元素形成的氧化物中,常见氧化物有CO2、SO3或NO2 , 、Na2O2 , BC为氯化物,则E为Cl2 , 如P有神形成三氯化磷、五氯化磷等,
(1.)符合转化关系的可以是碳单质,C ![]() CO
CO ![]() CO2 , 所以答案是:C,CO,CO2;
CO2 , 所以答案是:C,CO,CO2;
(2.)符合转化关系的可以是硫单质,S ![]() SO2
SO2 ![]() SO3 , 所以答案是:S,SO2 , SO3;
SO3 , 所以答案是:S,SO2 , SO3;
(3.)符合转化关系的可以是氮气单质,N2 ![]() NO
NO ![]() NO2 , 所以答案是;N2 , NO,NO2;
NO2 , 所以答案是;N2 , NO,NO2;
(4.)符合转化关系的可以是金属钠,Na ![]() Na2O
Na2O ![]() Na2O2 , 所以答案是:Na,Na2O,Na2O2;
Na2O2 , 所以答案是:Na,Na2O,Na2O2;


科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学通过查阅资料,获得了草酸的一些信息,整理出下表。
结构简式 | HOOC-OOH |
溶解性 | 能溶于水,易溶于乙醇 |
特性 | 大约在157℃升华(175℃以上发生分解) |
化学性质 | H2C2O4+Ca(OH)2=CaC2O4↓+2H2O |
HOOC-COOH | |
2KMnO4+5H2C2O4+3H2SO4= K2SO4+2MnSO4+10CO2↑+8H2O |
(1)该组同学欲通过实验验证草酸受热分解产物中的CO2和CO(装置符合气密性要求,其他试剂可选)。

①填写表中空内。
仪器 | A | B | C |
加入试剂 | ________ | ________ | NaOH溶液 |
②简述检验CO的实验方法和实验现象__________________。
(2)实验室常用草酸钠测定KMnO4溶液的浓度。
①准确称取2.680g草酸钠,溶于稀硫酸和水制成100.0 mL溶液,每次取20.00mL溶液于锥形瓶中;将待测KMnO4溶液置于_______________(填“酸式”或“碱式”)滴定管中进行滴定。重复上述滴定操作三次,实验数椐如下表所示。待测KMnO4溶液的物质的量浓度为____________。
滴定前均为 | 第一次终点 | 第二次终点 | 第三次终点 | |
滴定管液面刻度 | 0.00 mL | 20.02mL | 21.00mL | 19.98mL |
②将酸性KMnO4溶液和H2C2O4溶液混合后,发现开始时溶液褪色不明显,但不久后迅速褪色,针对该实验现象,某同学认为KMnO4溶液与H2C2O4溶液的反应是放热反应,导致溶液温度升高,反应速率加快。你猜想还有可能是_____________的影响。若用实验证明你的猜想,除KMnO4溶液、H2C2O4溶液、稀硫酸外,还需要选择的合理试剂是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G![]() B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:![]() ,F中的E元素的质量分数为60%.回答问题:
,F中的E元素的质量分数为60%.回答问题:

(1)①中反应的化学方程式为 ;
(2)化合物Ⅰ的电子式为 ,它的空间构型是 ;
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量(写出离子方程式和计算过程);
(4)C与过量NaOH溶液反应的离子方程式为 ,反应后溶液与过量化合物Ⅰ反应的离子方程式为 ;
(5)E在I中燃烧观察到的现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图装置(Ⅰ)是一种可充电电池,装置(Ⅱ)为电解池。装置(Ⅰ)的离子交换膜只允许Na+通过,已知电池充、放电的化学方程式为2Na2S2+NaBr3![]() Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是
Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是
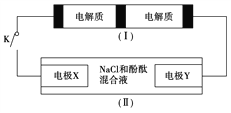
A. 闭合开关K时,Na+从右到左通过离子交换膜
B. 闭合开关K时,负极反应式为3NaBr-2e-===NaBr3+2Na+
C. 闭合开关K时,当有0.1 mol Na+通过离子交换膜时,X电极上放出标准状况下气体1.12 L
D. 闭合开关K时,X电极反应式为2Cl--2e-===Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,某溶液中含有Na+、H+、Fe3+、![]() 、OH-、I-中的几种离子,已知由水电离出的c(H+)=1×10-13 mol·L-1。向该溶液中缓慢通入一定量的Cl2后,溶液由无色变为黄色。下列关于该溶液的分析,错误的是
、OH-、I-中的几种离子,已知由水电离出的c(H+)=1×10-13 mol·L-1。向该溶液中缓慢通入一定量的Cl2后,溶液由无色变为黄色。下列关于该溶液的分析,错误的是
A. pH=1或pH=13
B. 阴离子肯定有I-,不能确定有无![]()
C. 阳离子肯定没有Fe3+,不能确定有无Na+
D. 溶质有3种可能:①HI ②HI和NaI ③NaI和NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学对电化学原理进行了一系列探究活动。
(1)如图为某实验小组依据氧化还原反应:(用离子方程式表示)__________________,设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________mol电子。

(2)用吸管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式___________,然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制饱和氯水,颜色褪去,同学们对此做了多种假设,某同学的假设是:“溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeO![]() ,试写出该反应的离子方程式____________________。
,试写出该反应的离子方程式____________________。
(3)如图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示。一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是溶液变红,电极反应为______________;乙装置中石墨(1)为________极(填“正”、“负”、“阴”或“阳”),乙装置中与铜丝相连石墨电极上发生的反应式为________________。

(4)观察如图所示的两个装置,图1装置中铜电极上产生大量的无色气泡,图2装置中铜电极上无气体产生,而铬电极上产生大量的有色气体。根据上述现象试推测金属铬具有的两种重要化学性质为__________________________、__________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将磷矿石〔Ca5(PO4)3F〕加工成过磷酸钙的主要目的是( )
A.增加磷的质量分数
B.使它性质稳定,便于贮存、运输
C.使它转化为较易溶于水的物质
D.施用时肥分不易流失
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com