
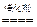 4NO+6H2O
4NO+6H2O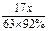
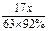
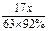 )×98% x
)×98% x

科目:高中化学 来源:不详 题型:单选题
| A.②③⑥ | B.①⑤⑦ | C.①④ | D.只有④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
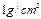 ,烧瓶内水溶液产生的蒸气压为
,烧瓶内水溶液产生的蒸气压为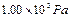 ,试求烧瓶中残留气体的压强为多少Pa?(设外界大气压为
,试求烧瓶中残留气体的压强为多少Pa?(设外界大气压为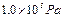 ,
,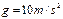 )
)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氮气 | B.二氧化碳 | C.空气 | D.氧气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 同时通入倒立于水中且盛满水的容器内,充分反应后,容器内残留
同时通入倒立于水中且盛满水的容器内,充分反应后,容器内残留 体积的气体,该气体与空气接触变为红棕色,则m与n的比值为:()
体积的气体,该气体与空气接触变为红棕色,则m与n的比值为:()| A.3∶2 | B.2∶3 | C.8∶3 | D.3∶8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com