
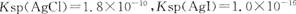 。下列关于不溶物之间转化的说法中正确的是 ( )
。下列关于不溶物之间转化的说法中正确的是 ( )A.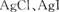 两者都不溶于水,因此AgCl与AgI不能相互转化 两者都不溶于水,因此AgCl与AgI不能相互转化 |
B.常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于 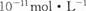 |
| C.一定条件下AgCl可以转化为更难溶的AgI |
| D.只能由Ksp较大的不溶物转化为Ksp较小的不溶物 |
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案科目:高中化学 来源:不详 题型:计算题
| A.将难溶电解质放入纯水中,溶解达到平衡时,升高温度, Ksp 一定增大 |
| B.两种难溶盐电解质,其中Ksp小的溶解度也一定小 |
| C.难溶盐电解质的Ksp与温度有关 |
| D.向AgCl的悬浊液中加入适量的水,使AgCl再次达到溶解平衡,AgCl的Ksp不变,其溶解度也不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.水垢的主要成分是MgCO3和CaCO3 |
| B.硬水的软化是将全部的Mg2+、Ca2+除尽 |
| C.加入FeS、MnS以除去工业废水中的Cu2+、Cd2+、Pb2+等重金属离子 |
| D.胃舒平的主要成份是氢氧化铁,可治疗胃酸过量,同时也可补铁。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②③④ | B.①②③ | C.③④⑤ | D.全部 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.8×10-9mol?L-1 | B.1.8×10-10mol?L-1 |
| C.5.9×10-10mol?L-1 | D.5.9×10-9mol?L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.
| B.
| C.14+
| D.14+
|
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| K甲/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
| A.向该混合溶液中加入少量铁粉,立即能观察到有红色固体析出 |
| B.向该混合溶液中逐滴加入NaOH溶液,最先看到蓝色沉淀 |
| C.该混合溶液中c(SO42-):{c(Cu2+)+c(Fe2+)+c(Fe3+)}>5:4 |
| D.向该混合溶液中加入适量氯水,并调节溶液的pH为3-4,然后过滤,可得到纯净的CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
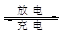 Fe2++Cr3+。下列说法一定正确的是
Fe2++Cr3+。下列说法一定正确的是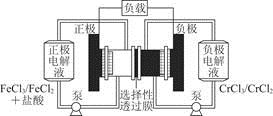
| A.充电时,阴极的电极反应式为Cr3++e-=Cr2+ |
| B.电池放电时,负极的电极反应式为Fe2+-e-=Fe3+ |
| C.电池放电时,Cl-从负极室穿过选择性透过膜移向正极室 |
| D.放电时,电路中每流过0.1 mol电子,Fe3+浓度降低0.1 mol·L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com