
【题目】工业上以铬铁矿(含有Cr2O3,FeO、Al2O3、SiO2等成分)为主要原料生产重铬酸钠晶体(Na2Cr2O7·2H2O),其主要工艺流程如下:
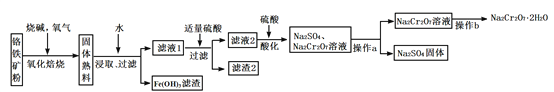
提示:熟料中含有Na2CrO4、NaFeO2等成分。
回答下列问题:
(1)将铬铁矿粉碎的目的是_____________________________ 。
(2)氧化焙烧时,生成Na2CrO4的化学方程式是__________。
(3)滤渣2中除Al(OH)3外还有__________(填化学式)。
(4)加入硫酸酸化的目的是__________________________。
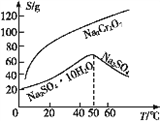
(5)根据下图,请将操作a补充完整:________________,洗涤,干燥。
(6)控制105~110℃,向较浓的Na2Cr2O7溶液中加入KCl固体发生复分解反应,立即析出K2Cr2O7晶体。能生成K2Cr2O7晶体的原因是_____________。
(7)向Na2Cr2O7酸性溶液中加入过量FeSO4溶液,生成Cr3+和 Fe3+,再加入过量的强碱溶液生成铁铬氧体沉淀(CrxFe3-xO4)。加入过量强碱生成铁铬氧体沉淀的离子方程式是______。
【答案】 增大反应物的接触面,加快反应速率,提高原料的利用率。 2Cr2O3 + 3O2 + 8NaOH![]() 4Na2CrO4 + 4H2O H2SiO3 将Na2CrO4转化为Na2Cr2O7。 蒸发浓缩,趁热过滤 该温度下,KCl、Na2Cr2O7、K2Cr2O7、NaCl四种物质中K2Cr2O7溶解度最小。 xCr3+ + Fe2+ + (2-x) Fe3+ +8OH-
4Na2CrO4 + 4H2O H2SiO3 将Na2CrO4转化为Na2Cr2O7。 蒸发浓缩,趁热过滤 该温度下,KCl、Na2Cr2O7、K2Cr2O7、NaCl四种物质中K2Cr2O7溶解度最小。 xCr3+ + Fe2+ + (2-x) Fe3+ +8OH-![]() CrxFe3-xO4↓+ 4H2O
CrxFe3-xO4↓+ 4H2O
【解析】试题分析:(1)将铬铁矿粉碎可以增大反应物的接触面,加快反应速率,提高原料的利用率;(2)氧化焙烧时Cr2O3被氧气氧化为Na2CrO4;(3)矿石中SiO2焙烧生成硅酸钠,加入硫酸生成硅酸;(4)Na2CrO4在酸性条件下生成Na2Cr2O7;(5)根据下图,请将操作a补充完整:________________,洗涤,干燥。(6)相同温度下,KCl、Na2Cr2O7、K2Cr2O7、NaCl四种物质中K2Cr2O7溶解度最小,析出K2Cr2O7沉淀;(7)加入过量强碱生成铁铬氧体沉淀,根据元素守恒;电荷守恒配平离子方程式。
解析:(1)将铬铁矿粉碎的目的是增大反应物的接触面,加快反应速率,提高原料的利用率;(2)氧化焙烧时Cr2O3被氧气氧化为Na2CrO4,反应方程式为2Cr2O3 + 3O2 + 8NaOH![]() 4Na2CrO4 + 4H2O ;(3)矿石中SiO2焙烧生成硅酸钠,加入硫酸生成硅酸,所以滤渣2中除Al(OH)3外还有H2SiO3沉淀;(4)Na2CrO4在酸性条件下能生成Na2Cr2O7,加入硫酸酸化的目的是将Na2CrO4转化为Na2Cr2O7;(5)根据硫酸钠在高温条件下溶解度比重铬酸钠小很多,所以混合溶液中析出硫酸钠晶体,步骤是蒸发浓缩,趁热过滤,洗涤,干燥。(6)相同温度下,KCl、Na2Cr2O7、K2Cr2O7、NaCl四种物质中K2Cr2O7溶解度最小,所以能生成K2Cr2O7晶体;(7)根据元素守恒;电荷守恒配平离子方程式得xCr3+ + Fe2+ + (2-x) Fe3+ +8OH-
4Na2CrO4 + 4H2O ;(3)矿石中SiO2焙烧生成硅酸钠,加入硫酸生成硅酸,所以滤渣2中除Al(OH)3外还有H2SiO3沉淀;(4)Na2CrO4在酸性条件下能生成Na2Cr2O7,加入硫酸酸化的目的是将Na2CrO4转化为Na2Cr2O7;(5)根据硫酸钠在高温条件下溶解度比重铬酸钠小很多,所以混合溶液中析出硫酸钠晶体,步骤是蒸发浓缩,趁热过滤,洗涤,干燥。(6)相同温度下,KCl、Na2Cr2O7、K2Cr2O7、NaCl四种物质中K2Cr2O7溶解度最小,所以能生成K2Cr2O7晶体;(7)根据元素守恒;电荷守恒配平离子方程式得xCr3+ + Fe2+ + (2-x) Fe3+ +8OH-![]() CrxFe3-xO4↓+ 4H2O。
CrxFe3-xO4↓+ 4H2O。


科目:高中化学 来源: 题型:
【题目】下列关于晶体的叙述错误的是
A.在金刚石网状结构中,由共价键形成的最小碳环上有6个碳原子
B.在氯化钠晶体中,每个钠离子的周围与它最近且等距离的钠离子有12个
C.在干冰晶体中,每个二氧化碳分子周围距离最近且相等的二氧化碳分子数是12
D.在氯化铯的晶体中,每个铯离子的周围与它最近且等距离的铯离子有8个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒容密闭容器中存在下列平衡:CO(g)+H2O(g)![]() CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如右图所示。下列说法错误的是
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如右图所示。下列说法错误的是

A. 在T2时,若反应进行到状态D,则一定有v正<v逆
B. 平衡状态A与C相比,平衡状态A的c(CO)小
C. 若T1、T2时的平衡常数分别为K1、K2,则K1<K2
D. 反应CO(g)+H2O(g)![]() CO2(g)+H2(g)的△H>0
CO2(g)+H2(g)的△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
合成氨的反应中的能量变化如图所示。
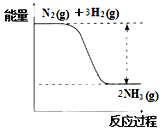
①该反应是___________反应(填“吸热”或“放热”),其原因是反应物化学键断裂吸收的总能量_____(填“大于”或“小于”)生成物化学键形成放出的总能量。
②在一定条件下,将一定量的N2和H2的混合气体充入某定容密闭容器中,一段时间后,下列叙述不能说明该反应达到平衡状态的是___________(填序号)。
A.容器中混合气体的密度不随时间变化
B.单位时间内断裂3 mol H-H键的同时断裂6 mol N-H键
C.N2 、H2 、NH3的物质的量之比为1:3:2
D.容器中混合气体的平均相对分子质量不随时间变化
③一种用于驱动潜艇的液氨-液氧燃料电池原理示意如图:
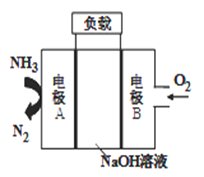
电极A上发生的电极反应为:_____________________。
若电池工作一段时间后,消耗标准状况下的氧气11.2L,则该过程转移电子______mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:短周期元素A、B、C、D、E的原子序数依次增大。
①C的简单气态氢化物遇湿润的红色石蕊试纸变蓝色;
②A与D可以形成原子个数比分别为2∶1、1∶1的两种液态化合物X和Y,A、E同主族,C与B、D相邻;
③A、B、C、D四种元素组成一种化合物F,其组成原子数之比为5∶1∶1∶3。
请回答下列问题:
(1)C原子在周期表的位置为___________;写出化合物EDA的电子式________。
(2)C的最高价氧化物对应的水化物与其气态氢化物反应可生成盐,写出其化学式________;
(3)F溶液与足量EDA的稀溶液混合加热,其离子方程式为_____________________。
(4)氯气与C的简单气态氢化物相遇有白烟及C2生成,写出反应方程式_____________。
(5)用CH4可以消除汽车尾气中氮氧化物的污染。
已知:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(l) ΔH=-955 kJ·mol-1
N2(g)+CO2(g)+2H2O(l) ΔH=-955 kJ·mol-1
2NO2(g)![]() N2O4(g) ΔH=-56.9 kJ·mol-1
N2O4(g) ΔH=-56.9 kJ·mol-1
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化亚铜(CuBr)常用作有机合成原料和反应催化剂等,它是一种不溶于水的白色结晶粉末,受热或见光易分解,接触空气会被缓慢氧化成绿色粉末。制备CuBr的实验步骤如下:
步骤1:在如图所示的三颈烧瓶中加入45gCuSO4·5H2O、19gNaBr、150mL煮沸过的蒸馏水,60℃时不断搅拌,以适当流速通入SO22小时。
步骤2:溶液冷却后倾去上层清液,在避光的条件下过滤。
步骤3:依次用溶有少量SO2的水、溶有少量SO2的乙醇、纯乙醚洗涤。
步骤4:将获得的产品经系列干燥剂干燥后,再进行真空干燥。

请根据上述制备步骤回答有关问题:
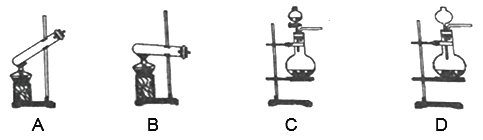
(1)制备中用到的SO2在实验室中通常是用浓硫酸和亚硫酸钠为原料来制备的,在制备SO2时装置可以选择下图中的____________(填装置编号),发生反应的化学方程式为____________。
(2)步骤1中:①所用蒸馏水需提前煮沸处理,这样做的目的是____________。
②为控制反应在60℃进行可采取的措施是________________。
③三颈烧瓶中反应生成CuBr的离子方程式为_____________。
④判断反应已经完成的现象是______________。
(3)步骤2在过滤时需要避光的原因是___________。
(4)步骤3中用到的洗涤剂水、乙醇中均“溶有少量SO2”的原因是____________。
(5)欲利用上述装置烧杯中的吸收液(经检测主要含Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。需用到以下试剂:SO2(贮存在钢瓶中)、100g20%NaOH溶液、乙醇等。请将下列实验步骤补充完整。
①向烧杯中继续通入SO2至溶液饱和;②____________;③加入少量维生素C溶液(抗氧化剂),蒸发浓缩,冷却结晶;④______________;⑤放真空干燥箱中干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、社会发展息息相关,下列有关说法不正确的是
A. “霾尘积聚难见路人”,霾尘所形成的气溶胶有丁达尔效应
B. “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
C. “青蒿一握,以水二升渍,绞取汁”,此法对青蒿素的提取属于化学变化
D. 古剑“沈卢”“以剂钢为刃,柔铁为茎干”,剂钢指的是铁的合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
A. 增大压强 B. 升高温度 C. 使用催化剂 D. 多充O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com