
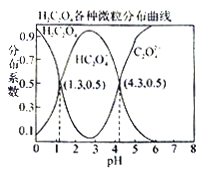
����Ŀ�������£�0.1 mol/L��H2C2O4��Һ��H2C2O4��HC2O4-��C2O42-��������ռ���ʵ����������ֲ�ϵ������pH�仯�Ĺ�ϵ��ͼ��ʾ�����б�������ȷ����
A. HC2O4-![]() H+��C2O42-��K��1��10-4.3
H+��C2O42-��K��1��10-4.3
B. �������ʵ�����NaHC2O4��Na2C2O4����ˮ�У�������ҺpHǡ��Ϊ4.3
C. ������HF��K��1��10-3.45��������H2C2O4��Һ���뵽����NaF��Һ�У������ķ�ӦΪ��H2C2O4+F-=HF��HC2O4-
D. ��0.1 mol/LNaHC2O4��Һ�У�������Ũ�ȴ�С��ϵΪ��c(Na+)��c(HC2O4-)��c(H+)��c(C2O42-)��c(OH-)
���𰸡�B
��������A����HC2O4-H++C2O42-����֪K=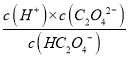 ��pH=4.3ʱ��c(C2O42-)=c(HC2O4-)������K=
��pH=4.3ʱ��c(C2O42-)=c(HC2O4-)������K=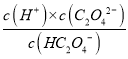 =c(H+)=1��10-4.3����A��ȷ��B���������ʵ�����NaHC2O4��Na2C2O4����ˮ�У�HC2O4-����̶ȴ���C2O42-��ˮ��̶ȣ�������Һ��c(C2O42-)��c(HC2O4-)������ҺPH����4.3����B����C��������H2C2O4��K1=10-1.3��K2=10-4.3��HF��KB=1��10-3.45�������ԣ�H2C2O4��HF��HC2O4-�����Խ�����H2C2O4��Һ���뵽����NaF��Һ�У������ķ�ӦΪH2C2O4+F-=HF+HC2O4-����C��ȷ��D��NaHC2O4��Һ�����ԣ���HC2O4-�ĵ���Ϊ��������Һ�в��ֵ���HC2O4-���������Ũ�ȴ�С��ϵΪ��c(Na+)��c(HC2O4-)��c(C2O42-)��c(OH-)����D��ȷ����ѡB��
=c(H+)=1��10-4.3����A��ȷ��B���������ʵ�����NaHC2O4��Na2C2O4����ˮ�У�HC2O4-����̶ȴ���C2O42-��ˮ��̶ȣ�������Һ��c(C2O42-)��c(HC2O4-)������ҺPH����4.3����B����C��������H2C2O4��K1=10-1.3��K2=10-4.3��HF��KB=1��10-3.45�������ԣ�H2C2O4��HF��HC2O4-�����Խ�����H2C2O4��Һ���뵽����NaF��Һ�У������ķ�ӦΪH2C2O4+F-=HF+HC2O4-����C��ȷ��D��NaHC2O4��Һ�����ԣ���HC2O4-�ĵ���Ϊ��������Һ�в��ֵ���HC2O4-���������Ũ�ȴ�С��ϵΪ��c(Na+)��c(HC2O4-)��c(C2O42-)��c(OH-)����D��ȷ����ѡB��


 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2015��˹̹����ѧ�о���Ա���Ƴ�һ�ֿ���һ��������ɳ�ŵ�ij������������ӵ�����ڲ���AlCl4�C���л������ӹ��ɵ������Һ����ŵ繤��ԭ������ͼ��ʾ������˵������ȷ����
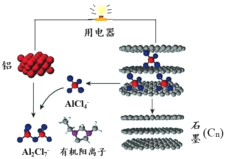
A���ŵ�ʱ����Ϊ������ʯīΪ����
B���ŵ�ʱ���л������������缫�����ƶ�
C���ŵ�ʱ�ĸ�����ӦΪ��Al �C3e- + 7AlCl4�C = 4Al2Cl7�C
D�����ʱ��������ӦΪ��Cn + AlCl4�C�Ce- = CnAlCl4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��̬��1���ֻ����1���Cl2�����ӳɷ�Ӧ�������ȴ����������ȴ�����1mol����4molCl2������ȫȡ����Ӧ��������Ľṹ��ʽΪ
A. CH2=CH2 B. CH3CH=CH2 C. CH3CH3 D. CH3CH2CH=CH2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Ũ�������������ȷ���ǣ� ��
A.Ũ���������ˮ�ԣ������ʹ����̿��
B.Ũ�����ڳ����¿�Ѹ����ͭƬ��Ӧ�ų�������������
C.Ũ������һ�ָ�������ܹ����ﰱ��������������
D.Ũ�����ڳ������ܹ�ʹ�������Ƚ����ۻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȥNa2CO3 ����������NaHCO3����ѷ����ǣ� ��
A�������������� B������NaOH��Һ C������ D�������Һ��ͨ��CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ĵ��ӽṹ�У���һ��������С��ԭ�ӿ����ǣ� ��
A. ns2np3B. ns2np4C. ns2np5D. ns2np6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʯ����Ȼ������ʯ������ͨ�����·�Ӧ����Ӧ��������֪���Ļ�ѧʽ������A~J����ѧ��ѧ�еij������ʣ�G��һ�ֺ��ɫ���壬D��һ��������ˮ�ĺ����ᣬJ��һ����Ҫ���������壬A����ɫ��Ӧ�ʻ�ɫ��E��B�ֱ����ữ����������Һ��Ӧʱ��ʵ��������ͬ�����а�ɫ������������ʵ���������ʯ��Ħ������Ϊ204g ��mol��1��������Ԫ�ص���������Ϊ54.9%�������еIJ�������������ȥ��

�ش��������⣺
��1��A�ĵ���ʽ_____________��
��2�������ʯ�Ļ�ѧʽ_____________��
��3��д��C��F�����ӷ���ʽ_____________��
��4��д��H��G�Ļ�ѧ����ʽ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��Ϊ̽��AgNO3��Һ�Ͳ�ͬ��������Һ��Ӧ�Ķ����ԣ��������ʵ�飺

��֪��AgSCNΪ��ɫ�����(SCN)2��±�������������ƣ�(SCN)2Ϊ��ɫ���ʡ�
��1�����еİ�ɫ������___________________��
��2�����벢ϴ�Ӣٵij������μ�0.5mol/L KI��Һ����ɫ����ת��Ϊ��ɫ�����������ӷ���ʽ���������仯____________________________��
��3�����п���������������Ӧ��_________________��
��4��ʵ��ٵ����Ŀ��_______________________��
��5�����ڢ��к�ɫ��ȥ��ԭ����Ag+��SCN����Ӧ�������С��������·�������ƣ�
��.��ͬѧ��Ϊ����ɫ��ȥ��ԭ����ƽ���ƶ�ԭ���йأ�����Ϊ_________________��
��.��ͬѧΪ��̽�������Ƿ���Ag+����SCN���ķ�Ӧ����������¶Ա�ʵ�飺

�������ɰ�ɫ��������ʱ��۲죬��Һ�ͳ�����δ������ɫ�ı䡣
��.��ͬѧ��Ϊ��������Ag+�ܹ�����SCN����Ϊ֤������룬�������ʵ����

��������ָ�뷢��ƫת��a�缫�ϲ������н�����������ʣ�b�缫��������Һ������ɫ�仯��
��ͬѧ�������֤��������ԭ��Ӧ���ŵ���___________________________��
��6��ͨ������̽�����ó�AgNO3��Һ�Ͳ�ͬ��������Һ��Ӧ�����ԵĽ�����______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com