
 �й�������ϯ���������зǺ�����̳��������ϳ�ŵ�����ṩ3��Ԫ�������Ԯ�����������ű���������ṩ������ҩƷ������30����ű���ġ����й����Ƴɹ���ȫ��Ψһ������ű����Чҩ--�����أ���������������еġ��й���ҩ�����ṹ��ͼ��ʾ��Ŀǰ�ۼ�ÿ��225��Ԫ�����������15�֣�����������ʮ��֮һ������Ӧ�����й��������ص�˵����ȷ���ǣ�������
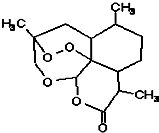
�й�������ϯ���������зǺ�����̳��������ϳ�ŵ�����ṩ3��Ԫ�������Ԯ�����������ű���������ṩ������ҩƷ������30����ű���ġ����й����Ƴɹ���ȫ��Ψһ������ű����Чҩ--�����أ���������������еġ��й���ҩ�����ṹ��ͼ��ʾ��Ŀǰ�ۼ�ÿ��225��Ԫ�����������15�֣�����������ʮ��֮һ������Ӧ�����й��������ص�˵����ȷ���ǣ�������| A����һ���� |
| B�����ڸ߷��ӻ����� |
| C�����ڷ����廯���� |
| D������ʽ��C15H22O5 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
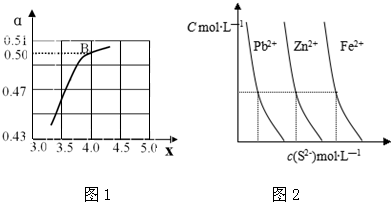
| n(NH3) |
| n(CO2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶� | 250��C | 300��C | 350��C |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��SO2��CO2����ɡ����ꡱ��������� |
| B����ˮ����������ˮ�и�����Ԫ����ɵ� |
| C�����⻯ѧ��������NO2���ŷ��й� |
| D��ȼ����Ҷ��������������ɴ�����Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��AlCl3��Һ�м������Ũ��ˮ��Al3++3NH3?H2O�TAl��OH��3��+3NH4+ | ||||
| B��������ˮ��Ӧ��Cl2+H2O=2H++Cl-+ClO- | ||||
C���Ȼ�狀���ʯ�ҹ�����������ư��������ӷ���ʽ��NH4++OH-
| ||||
| D��Cu��������ϡ���Cu+2NO3-+4H+�TCu2++2NO2��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
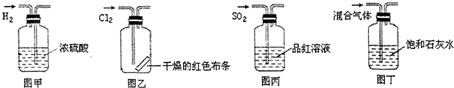
| A��ͼ����ʾ���ɵõ���������� |
| B��ͼ����ʾ��������֤������Ư���� |
| C��ͼ����ʾ��������֤SO2��Ư���� |
| D��ͼ����ʾ����ʯ��ˮ����ǣ�֤�����������һ������CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ �� �� ʵ | �� �� | |
| A | A��B�����л��������ͬ����Է��������Ͳ�ͬ�Ľṹ | A��B��Ϊͬ���칹�� |
| B | ������ͬ��A��B�����л�����ȫȼ������������ͬ��ˮ | A��B���л������ʽ��ͬ |
| C | A��B�����л���ṹ���ƾ�����ͬ��ͨʽ | A��B��Ϊͬϵ�� |
| D | ����ʽΪC6H6����A����ʹ���CCl4��Һ��ɫ������ʹ����KMnO4��Һ��ɫ | A�Ľṹ��ʽ������ CH2�TCH��C-CH�TCH2 |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NO2��NO3- |
| B��SO2��SO3 |
| C��Cl2��NaClO |
| D��Fe3+��Fe2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ba��OH��2��Һ����μ���NH4HSO4��Һ���պó�����ȫ��Ba2++2OH-+H++SO42-+NH4+�TBaSO4��+NH3?H2O+H2O |
| B��������þ��ɫ���������Ȼ����Һ��Mg��OH��2+2NH4+�TMg2++2NH3?H2O |
| C�����Ƶ�ˮ�⣺S2-+2H2O�TH2S+2OH- |
| D��NaHCO3��Һ�еμ���������ʯ��ˮ��2HCO3-+Ca2++2OH-�TCaCO3��+2H2O+CO32- |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com