
����Ŀ����д���пհף�
(1)��֪ijԭ�ӵĺ�����77�����ӣ�������Ϊ191��������ڵ�������Ϊ_________��
(2)���ڱ���λ�ڵ�8���е���Ԫ�����ڵ�________�塣
(3)���ڱ�������õķǽ���Ԫ��λ�ڵ�_____________���С�
(4)����Ԫ��Ϊ18�ֵ������ǵ�____________���ڡ�
(5)4g D2��20g 18O�ĵ��ʻ���ʱ���������_______g D2O����ЩD2O�����к�___mol���ӡ�
(6)��Ԫ������Ȼ������������Ϊ35��37�����ֺ��أ���Ԫ�ص����ԭ������Ϊ35.5��������������Ȼ���еĺ���֮��ԼΪ______________��
���𰸡�114 �� 17 �ġ��� 22 12 3:1
��������
(1)ԭ����������+������=��������
(2)Ԫ�����ڱ��еĵ�8��9��10��������Ϊ�����壻
(3)Ԫ�����ڱ��й���18�����У�
(4)һ��������Ԫ�ص��������ֱ�Ϊ2��8��8��18��18��32��26��
(5)�ȸ���4gD2�������Ҫ�������������жϳ������������ķ�Ӧ������ټ�������ˮ��������һ��ˮ�����к���12�����ӣ��ݴ˼������ӵ�����
(6)������ƽ�����ԭ����������������Ȼ���еĺ���֮�ȡ�
(1)ԭ�ӵĺ�����77�����ӣ�������Ϊ191����������=191-77=114���ʴ�Ϊ��114��
(2)����Ԫ�������ڱ��д��ڵ�8���У���8��9��10��������Ϊ�����壬�ʴ�Ϊ������
(3)���ڱ�������õķǽ���Ԫ��ΪF��Ϊ����A��Ԫ�أ������һ��Ԫ�����ڣ���λ�ڵ�17���У��ʴ�Ϊ��17��
(4)һ��������Ԫ�ص�����ֱ�Ϊ2��8��8��18��18��32��26(δ����������Ϊ32)��������Ԫ��Ϊ18�ֵ������ǵ��ġ������ڣ��ʴ�Ϊ���ġ��壻
(5)4gD2�����ʵ���Ϊ![]() =1mol������ʱ��Ҫ����(18O2)������Ϊ1mol��
=1mol������ʱ��Ҫ����(18O2)������Ϊ1mol��![]() ��36g/mol=18g��20g������������ʣ�࣬����������������4g���μӷ�Ӧ��������������18g��������ˮ��������22g��ˮ�����ʵ���=���������ʵ���=1mol��һ��ˮ�����к���1��2+(18-8)=12�����ӣ��������ӵ����ʵ�����12mol���ʴ�Ϊ��22��12��
��36g/mol=18g��20g������������ʣ�࣬����������������4g���μӷ�Ӧ��������������18g��������ˮ��������22g��ˮ�����ʵ���=���������ʵ���=1mol��һ��ˮ�����к���1��2+(18-8)=12�����ӣ��������ӵ����ʵ�����12mol���ʴ�Ϊ��22��12��
(6)��������Ϊ35��37��������Ԫ�صĺ�������Ȼ���еĺ����ֱ���x��y����Ԫ�ص����ԭ������Ϊ35.5����35.5=35x+37y��x+y=1�����x=0.75��y=0.25����x��y=3��1���ʴ�Ϊ��3��1��


 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��R��T��Q��W��Ԫ�����ڱ��е����λ��������ͼ��ʾ������ T ������������������������ȡ������жϲ���ȷ����
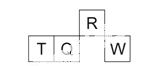
A. �����̬�⻯������ȶ��ԣ�R > Q
B. ����������Ӧˮ��������ԣ�Q < W
C. ԭ�Ӱ뾶��T > Q > R
D. �� T ������Һһ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ҵ��Һ�к���Cu2+��Mg2+��Zn2+�����ӣ�Ϊ����������ã����������¹���

��֪Zn��OH��2��������Al��OH��3���ƣ������Լ��������Լ���ѡ��
������ ��п�� ��ϡHNO3 ��ϡH2SO4 ��ϡHCl ��ϡ��ˮ ��NaOH��Һ ��ʯ��ˮ
��ش��������⣺
��1���Լ�1���Լ�2���Լ�3�ֱ������__________________�����ţ�
��2������2������______________ ��________________ �� __________
��3������3��________________________________
��4���ӹ���CO2ʱ������Ӧ�����ӷ���ʽ_________________________________
��5���ڽ���ұ�������з���1��______________����2��_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Be��OH��2�����Եģ���ǿ�ᷴӦʱ����Be2+����ǿ�Ӧʱ����BeO22�����������ݵ����ʵ���Ũ�ȡ��������BeCl2��MgCl2��AlCl3��Һ������ʱ�������������ᣩ���ֽ�һ��Ũ�ȵ�NaOH��Һ�ֱ����������Һ����������NaOH��Һ�����x��mL�������ɳ��������ʵ���y��mol���Ĺ�ϵ��ͼ��ʾ������BeCl2��MgCl2��AlCl3������Һ��Ӧ��ͼ����ȷ���ǣ�������

A. �ݢۢ� B. �ڢۢ� C. �ۢݢ� D. �ۢڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1L��0.01molNaAlO2��0.02molNaOH����Һ�л���ͨ�������̼����n(CO2)�����Ⱥ���������ͬ�ķ�Ӧ����0.01mol<n(CO2) ![]() 0.015ʱ�����ķ�Ӧ�ǣ�2 NaAlO2+ CO2+2H2O=2Al(OH)3��+Na2CO3���ж�Ӧ��ϵ��ȷ����( )
0.015ʱ�����ķ�Ӧ�ǣ�2 NaAlO2+ CO2+2H2O=2Al(OH)3��+Na2CO3���ж�Ӧ��ϵ��ȷ����( )
ѡ�� | n(CO2)/mol | ��Һ�����ӵ����ʵ���Ũ�� |
A | 0 | c(Na+)>c(AlO2-)+c(OH-) |
B | 0.01 | c(Na+)>c(AlO2-)> c(OH-)>c(CO32-) |
C | 0.015 | c(Na+)> c(HCO3-)>c(CO32-)> c(OH-) |
D | 0.03 | c(Na+)> c(HCO3-)> c(OH-)>c(H+) |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(��)A��B��C��D��E����Ԫ�������ڱ����λ�����±���ʾ��
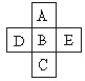
A��B��CΪͬ����Ԫ�أ�AΪ������ԭ�Ӱ뾶��С��Ԫ�أ�D��B��EΪͬ����Ԫ�أ�EΪ��������ԭ�Ӱ뾶��С��Ԫ�ء�DԪ��������____�������ڱ���___���ڣ���______�壬��ԭ�ӽṹʾ��ͼ______��
(��)A��B��C��D��E��F���ֶ�����Ԫ�ص�ԭ����������������֪A��C��F��ԭ�ӵ�����㹲��11�����ӣ���������Ԫ�ص�����������ˮ����֮���������ܷ�Ӧ���������κ�ˮ��DԪ��ԭ�ӵ������������ȴ�����������4����EԪ��ԭ�ӵĴ�����������������������3�����Իش�
(1)д������Ԫ�صķ���A_____��D_____��E_____��
(2)A��C����Ԫ������������ˮ����֮�䷴Ӧ�����ӷ���ʽ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪8NH3+3Cl26NH4Cl+N2,Ϊ��֤�ǽ���Ԫ���ȵ�������ǿ����͵�,�����һ��ʵ��װ��(���ּг�װ������ȥ):
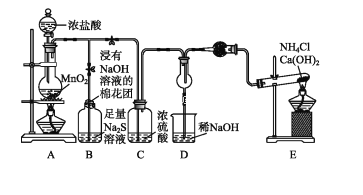
(1)д��E�з�Ӧ�Ļ�ѧ����ʽ_____��
(2)B�г��ֻ�ɫ��������,��������������ӷ���ʽ______________��
(3)D�и�����г��ֵ�������_______________��
(4)��ͬѧ��ΪD�е�������˵���ȵ������Դ��ڵ�,��Ҫ��C֮ǰ��װϴ��װ�ã���ָ��ϴ��װ��ʢװ�Լ�______��
(5)ͨ��Dװ�õ�����������߽϶̡��ұ߽ϳ���Ŀ����________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣���ش��й����⣺
| ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
4 | �� | �� |
(1)���л�ѧ��������õ�Ԫ�أ���ԭ�ӽṹʾ��ͼΪ ________ ��
(2)�������γ��������������Ԫ���� ________ (��Ԫ�ط��ű�ʾ)��д����Ԫ�صĵ�����������������ˮ���ﷴӦ�Ļ�ѧ����ʽ��_________��
(3)�ۢߢ�����Ԫ�ص������ӻ�ԭ��˳��Ϊ�� _________________�������ʵ�ˮ��Һ��__________ɫ��
(4)�١��ڡ��ޡ�������Ԫ�ص�����������ˮ������������ǿ���� _______(�����ʻ�ѧʽ) ��(��ʾ��ͬ����Ԫ�أ������ҷǽ���������ǿ��)
(5)��Ԫ������Ԫ�����ߺ˵����֮���� ____________ ��
(6)���ʵ�鷽�����Ƚ����������������Ե�ǿ�����뽫���������±���
ʵ�鲽�� | ʵ����������� |
____________________ | ____________________ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ͬ�ļס������������У��ֱ���е����ʵ�����SO2��O2������ͬ�¶��·�����Ӧ:2SO2+O2![]() 2SO3���ﵽƽ�⡣������һ�����У�����������������䣬����������ѹǿ���䣬����ڼס���������˵����ȷ���ǣ� ��
2SO3���ﵽƽ�⡣������һ�����У�����������������䣬����������ѹǿ���䣬����ڼס���������˵����ȷ���ǣ� ��
A. ��ƽ��ʱ��ױ��Ҷ�
B. ���������ٳ�������ʵ�����SO2��O2�����´�ƽ��ʱת���ʼ�С
C. ��ƽ��ʱ������SO2��Ũ�ȱ�����SO2��Ũ�ȴ�
D. ��ƽ��ʱ����ת���ʱ��ҵ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com