
| A.3.36 L | B.4.48 L | C.5.60 L | D.6.72 L |
科目:高中化学 来源:不详 题型:填空题
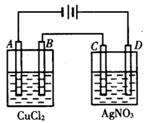
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.阴极只析出氢气 | B.阳极先析出氯气后析出氧气 |
| C.电解最后阶段为电解水 | D.电解过程中溶液的PH不断增大,最后pH为7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.4.48L | B.5.6L | C.6.72L | D.11.2L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 组号 | X | Y | Z | W |
| A | C | Fe | NaCl | H2O |
| B | Pt | Cu | CuSO4 | CuSO4溶液 |
| C | C | C | H2SO4 | H2O |
| D | Ag | Fe | AgNO3 | AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.b<a<7 |
| B.阴极电极反应式为:Cu2++2e-="Cu" |
| C.向溶液中加人9.8x(10-b-10-a)gCu(OH)2可使溶液恢复到电解前的浓度 |
| D.阳极产生的气体是O2,其体积(标准状况下)为1.12x(10-b-10-a)L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.35.5:108 | B.16:207 | C.108:35.5 | D. 8:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.2mol H2 | B.0.2mol Cl2 | C.0.4mol H2 | D.0.4mol Cl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=n | B.pH=-lg n | C.pH=14-lgn | D.pH=lgn+14 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com