

| A.等于1.369 g·L-1 | B.等于2.054 g·L-1 |
| C.在1.369 g·L-1和2.054 g·L-1之间 | D.大于2.054 g·L-1 |
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源:不详 题型:单选题
 C(g) DH<0,反应过程中温度保持不变。已知起始时V乙
C(g) DH<0,反应过程中温度保持不变。已知起始时V乙
 V甲,装置如下图所示。当反应达平衡时,测得甲中C的体积分数为40%。下列说法中不正确的是
V甲,装置如下图所示。当反应达平衡时,测得甲中C的体积分数为40%。下列说法中不正确的是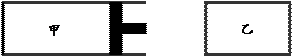
| A.容器甲、乙中反应的起始速率不等 |
| B.达平衡时,容器甲、乙中各组分的体积分数不等 |
| C.达平衡时,容器甲、乙中放出的热量相等 |
| D.达平衡时,容器乙中再充入少量稀有气体,A的转化率不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2O3,此时测知O2的转化率为30%,下列图象能正确表示气体的物质的量浓度(m)跟时间(t)的关系的是( )
2O3,此时测知O2的转化率为30%,下列图象能正确表示气体的物质的量浓度(m)跟时间(t)的关系的是( )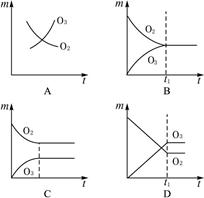
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g)(正反应为放热反应)达到平衡后,只改变一个条件时建立的新平衡的过程。填写下列各空(均填写图序号):
2NH3(g)(正反应为放热反应)达到平衡后,只改变一个条件时建立的新平衡的过程。填写下列各空(均填写图序号):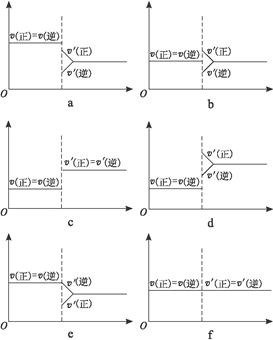
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g)+D(g)在恒温下已达平衡的标志是( )
C(g)+D(g)在恒温下已达平衡的标志是( )查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 PCl5(g)。达平衡后,PCl5为0.4mol。若此时再移走1mol PCl3和0.5mol Cl2,相同温度下重新达到平衡,PCl5的物质的量为( )
PCl5(g)。达平衡后,PCl5为0.4mol。若此时再移走1mol PCl3和0.5mol Cl2,相同温度下重新达到平衡,PCl5的物质的量为( )| A.0.4mol |
| B.0.2mol |
| C.0.2mol<x<0.4mol |
| D.<0.2mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 N2O3+O2,N2O3又按N2O3
N2O3+O2,N2O3又按N2O3 N2O+O2分解,在容积为1L的密闭容器中,将4molN2O5加热至t℃,达平衡时,氧气的浓度为4.5mol/L,N2O5的平衡浓度为1.7mol/L,则t℃时N2O5的平衡浓度应为( )
N2O+O2分解,在容积为1L的密闭容器中,将4molN2O5加热至t℃,达平衡时,氧气的浓度为4.5mol/L,N2O5的平衡浓度为1.7mol/L,则t℃时N2O5的平衡浓度应为( )| A.0.9mol/L | B.1.5mol/L | C.2.38mol/L | D.2.88mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 2NH3(g);ΔH="-92.4" kJ·mol-1。请回答:
2NH3(g);ΔH="-92.4" kJ·mol-1。请回答: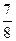 ,则N2的转化率a1= ,此时,反应放热 kJ;
,则N2的转化率a1= ,此时,反应放热 kJ;查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 NaCl(l)+K(g)-Q
NaCl(l)+K(g)-Q| 压强/kPa | 13.33 | 53.32 | 101.3 |
| K的沸点/℃ | 590 | 710 | 770 |
| Na的沸点/℃ | 700 | 830 | 890 |
| KCl的沸点/℃ | | | 1 437 |
| NaCl的沸点/℃ | | | 1 465 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com