
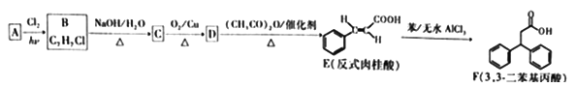
【题目】3,3-二苯基丙酸是一种医药中间体,某科技活动小组拟设计如下合成路线制备:
回答下列问题:
(1)A的名称为____________;B→C、E→F的反应类型分別为_________、________;参照E的结构和名称,反式对羟基肉桂醛的结构简式为_____________;F的分子式为_______________。
(2)C→D的化学方程式为_____________;D与(CH3CO)2O在催化剂作用下反应生成E,另一种产物的结构简式为______________。
(3)E的芳香族同分异构体中,含有碳碳双键,能与FeCl3溶液发生显色反应,还能发生银镜反应的共有_____________种(不含立体异构)。
(4)参照上述合成路线,以D、![]() 、苯为原料(无机试剂任选),设计制备
、苯为原料(无机试剂任选),设计制备 的合成路
的合成路
线______________________。
【答案】 甲苯 取代反应(或水解反应) 加成反应  C15H14O2
C15H14O2 ![]() CH3COOH 16
CH3COOH 16 
【解析】试题分析:根据B的分子式及E的结构简式,可知A是![]() 、B是
、B是 、C是
、C是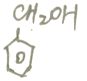 、D是
、D是 。
。
解析:⑴![]() 的名称为甲苯;
的名称为甲苯; →
→ 是氯原子被羟基代替,属于取代反应、
是氯原子被羟基代替,属于取代反应、 在双键两端分别连接氢原子和苯环,属于加成反应;参照E的结构和名称,反式对羟基肉桂醛的结构简式为
在双键两端分别连接氢原子和苯环,属于加成反应;参照E的结构和名称,反式对羟基肉桂醛的结构简式为 ;根据F的结构简式
;根据F的结构简式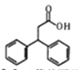 ,可知F的的分子式为C15H14O2。
,可知F的的分子式为C15H14O2。
(2)  氧化为
氧化为 的化学方程式为
的化学方程式为![]() ;
;  与(CH3CO)2O在催化剂作用下反应生成
与(CH3CO)2O在催化剂作用下反应生成![]() 和CH3COOH;
和CH3COOH;
(3)含有碳碳双键,能与FeCl3溶液发生显色反应,说明含有酚羟基,能发生银镜反应,说明含有醛基的E的同分异构体有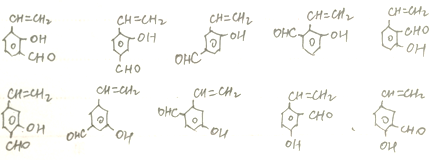 及
及 各有邻、间、对3种,共16种;
各有邻、间、对3种,共16种;
(4)根据上述合成路线,以 、
、![]() 、苯为原料(无机试剂任选),设计制备
、苯为原料(无机试剂任选),设计制备 的合成路线为
的合成路线为 。
。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】某有机物结构简式为 ,下列叙述不正确的是( )
,下列叙述不正确的是( )
A. 1 mol 该有机物在加热和催化剂作用下,最多能和4 mol H2反应
B. 该有机物能使溴水褪色,也能使酸性KMnO4溶液褪色
C. 该有机物遇硝酸银溶液产生白色沉淀
D. 该有机物在一定条件下能发生消去反应或取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧杯中各盛有100 mL 6 mol/L的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为1:2,则加入铝粉的质量为
A. 10.8g B. 7.2g C. 5.4g D. 3.6g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质递变情况错误的是
A. Li、Be、B原子最外层电子数逐渐增多 B. N、O、F原子半径依次增大
C. P、S、C1最高正价依次升高 D. Li、Na、K、Rb的金属性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取溴的工业流程如图:

(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是______.
(2)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的______.(填序号)
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)以上流程Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数及相应物质:_______
□Br2+□CO32-═□BrO3-+□Br-+□______
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴与二氧化硫水溶液反应的化学方程式:______.
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是______.(填序号)
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由ⅢA、VA族元素组成的新型材料有着广泛用途。
(1)B2H6是一种高能燃料,它与Cl2反应生成的BCl3可用于半导体掺杂工艺及高纯硅制造。与BCl3互为等电子体,且由第二周期元素组成的一种阴离子为__________(填离子符号)。
(2)氨硼烷(H3N—BH3)和Ti(BH4)3均为广受关注的新型化学氢化物储氢材料。
①H3N—BH3中N原子的轨道杂化类型为________________。
②Ti(BH4)3由TiCl3和LiBH4反应制得。基态Ti3+的未成对电子数为____________;BH4-的立体构型是_______;该制备反应的化学方程式为______________。
(3)氨硼烷可由六元环状化合物(HB=NH)3通过如下反应制得:
3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3。
下列有关叙述错误的是_____________
A.氨硼烷中存在配位键
B.第一电离能大小关系:N>O>C>B>H
C.反应前后碳原子的杂化类型不变
D.CH4、H2O、CO2分子空间构型分别是:正四面体型、V型、直线型
(3)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为_____________。Ga的配位原子(As)数目为________;Ga和As的摩尔质量分别为MGag·mol-1和MAsg·mol-1,原子半径分别为rGacm和rAscm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为__________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法正确的是

A. 对应简单离子半径:X>W
B. 对应气态氢化物的稳定性Y>Z
C. 化合物XZW既含离子键,又含共价键
D. Y的氧化物能与Z的氢化物和X的最高价氧化物对应的水化物的溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com