
 2NH3(g) △H=-92.4kJ/mol。
2NH3(g) △H=-92.4kJ/mol。 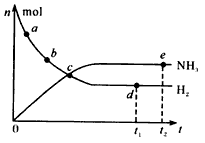
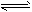 2NH3(g)的平衡常数K=____________。
2NH3(g)的平衡常数K=____________。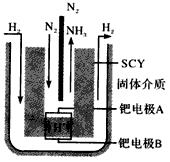
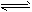 2NH3(g)+3/2O2(g) △H=akJ/mol进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
2NH3(g)+3/2O2(g) △H=akJ/mol进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表: 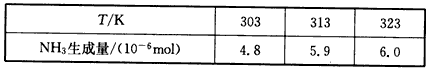
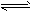 2NH3(g) △H=-92.4kJ/mol 2H2(g)+O2(g)=2H2O(l) △H=-571. 6kJ/mol
2NH3(g) △H=-92.4kJ/mol 2H2(g)+O2(g)=2H2O(l) △H=-571. 6kJ/mol  一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源:广东省高考真题 题型:填空题


 。设在容积为2.0 L的密 闭容器中充人0. 60 mol N2(g)和l.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。计算
。设在容积为2.0 L的密 闭容器中充人0. 60 mol N2(g)和l.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。计算  的平衡常数。
的平衡常数。 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com