
 ?
?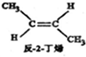 ,△H=-4.2kJ.mol-1
,△H=-4.2kJ.mol-1 (g)+H2(g)=CH3CH2CH2CH2(g),△=-118.9kJ.mol-1.
(g)+H2(g)=CH3CH2CH2CH2(g),△=-118.9kJ.mol-1.| A. | 反-2-丁烯比顺-2-丁烯稳定 | |
| B. | 顺-2-丁烯的燃烧热数值比反-2-丁烯小 | |
| C. | 减压和升温有利于平衡向生成正丁烷反应方向移动 | |
| D. | 反-2-丁烯氢化的热化学方程式为: (g)+H2(g)?CH3CH2CH2CH3(g),△H=-123.1kJ•mol-1 (g)+H2(g)?CH3CH2CH2CH3(g),△H=-123.1kJ•mol-1 |
分析 A.能量越低越稳定;
B.若生成物相同,反应物的能量高,则放出的热量多;
C.生成正丁烷的反应为气体体积减小的放热反应;
D.盖斯定律指若一个反应可以分步进行,则各步反应的吸收或放出的热量总和与这个反应一次发生时吸收或放出的热量相同.
解答 解:A.顺-2-丁烯转化为反-2-丁烯放热,说明反-2-丁烯能量低,更稳定,故A正确;
B.等量的顺-2-丁烯具有更高的能量.所以顺-2-丁烯燃烧热更大,故B错误;
C.生成正丁烷的反应为气体体积减小的放热反应,所以减压向逆向移动,升温也向逆向移动,所以减压和升温不利于平衡向生成正丁烷反应方向移动,故C错误;
D.将下式-上式相加得到反-2-丁烯氢化的热化学方程式,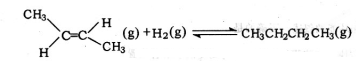 △H=-118.9kJ•mol-1-(-4.2kJ•mol-1)=-114.7kJ•mol-1,故D错误.
△H=-118.9kJ•mol-1-(-4.2kJ•mol-1)=-114.7kJ•mol-1,故D错误.
故选A.
点评 本题考查能量越低越稳定和盖斯定律、影响平衡的因素等,难度适中,注意掌握运用盖斯定律解题.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| t/s | 0 | 50 | 100 | 150 |
| c(X2O5)mol/L | 4.00 | 2.50 | 2.00 | 2.00 |
| A. | T温度下的平衡常数为K=64(mol/L)3,100s时转化率为50% | |
| B. | 50s内X2O5分解速率为0.03 mol/(L•s) | |
| C. | T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1>K2 | |
| D. | 若只将恒容改为恒压,其它条件都不变,则平衡时X2O5的转化率和平衡常数都不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 已知2SO2(g)+O2?2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 | |
| B. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知2C(s)+2O2(g)=2CO2 (g)△H1 2C(s)+O2(g)=2CO(g)△H2则△H1<△H2 | |
| D. | 已知H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol,则任何酸碱中和的反应热均为57.3kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下物质的量浓度相等①NH4HSO4、②(NH4)2SO4、③(NH4)2CO3三种溶液中c(NH4+) ①<②<③ | |
| B. | 在纯水中加入少量硫酸或硫酸铵,均可抑制水的电离 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaClO溶液中通入少量SO2:ClO-+SO2+H2O=2H++SO42-+Cl- | |
| B. | FeCl3溶液中通入过量H2S气体:2Fe3++3H2S=2FeS↓+S↓+6H+ | |
| C. | Na2CO3溶液中通入少量Cl2:2CO32-+Cl2+H2O=ClO-+Cl-+2HCO3- | |
| D. | NaHSO3溶液中通入少量Cl2:HSO3-+Cl2+H2O=3H++SO42-+2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Fe2(SO4)3•(NH4)2SO4•2H2O | B. | Fe2(SO4)3•2(NH4)2SO4•2H2O | ||
| C. | Fe2(SO4)3•2(NH4)2SO4•6H2O | D. | 2Fe2(SO4)3•(NH4)2SO4•6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com