


科目:高中化学 来源: 题型:单选题
| 选项 | 实验目的 | 玻璃容器 |
| A | 分离乙醇和乙酸乙酯的混合物 | 分液漏斗、烧杯 |
| B | 用pH=1的盐酸配制100mLpH=2的盐酸 | 100mL容量瓶、烧杯、玻璃棒、胶头滴管 |
| C | 用溴水、淀粉-KI溶液比较Br2与I2的氧化性强弱 | 试管、胶头滴管 |
| D | 用NH4Cl固体和Ca(OH)2固体制备并收集NH3 | 酒精灯、烧杯、导管、集气瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

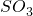 被
被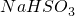 溶液吸收时产生了
溶液吸收时产生了 气体
气体查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 品 名 | ××× |
| 配 料 | 鲜鸡蛋、精面粉、白砂糖、精炼植物油、奶油、奶粉、食盐、柠檬汁等 |
| 保 质 期 | 240天 |
| 生产日期 | 标于包装袋封口上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com