
 ________HClO4
________HClO4 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.酸性强弱: H2SiO3<H2CO3<H2SO4<HClO4 |
| B.离子半径:Na+>Mg2+>Al3+>F- |
| C.碱性强弱:KOH>NaOH>Mg(OH)2>Al(OH)3 |
| D.热稳定性:HF>HCl>H2S>PH3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | | | | ① | ② | |
| ③ | | ④ | ⑤ | | ⑥ | ⑦ |
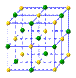
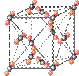
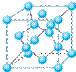
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验方案 | 实验现象 | ||||
| ①用砂纸打磨后的镁带与沸水反应,再向反应液中滴加酚酞。 ②向新制的H2S饱和溶液中滴加新制的氯水 ③钠与滴有酚酞试液的冷水反应 ④镁带与2mol/L的盐酸反应 ⑤铝条与2mol/L的盐酸反应 |
|
| 实验方案 | 实验现象 | 有关离子方程式 |
| | A | |
| | B | 不填 |
| | C | 不填 |
| | D | 不填 |
| | E | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X和Y都是性质活泼的元素,在自然界中只能以化合态存在 |
| B.X和Y形成的化合物的化学式为Y2X |
| C.X的最高正价为+6 |
| D.Y能置换酸中氢,放出氢气,但不能置换出盐中的金属 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| a | | | |||||||||||||||
| | | | | f | y | h | i | | |||||||||
| | b | | e | | | | j | | |||||||||
| c | | | | | | | d | | d | | g | | l | | | | |
| | | | | | | | | | | | | | | | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
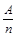 (K为A与n的比值)。下列推理正确的是
(K为A与n的比值)。下列推理正确的是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com