

分析 (1)可以用浓硫酸来干燥二氧化硫气体;SO3的熔点是16,8℃,较低,可以用冰水来获得三氧化硫,Ⅲ中为吸水和尾气处理;
(2)气体的制备及性质实验中需要检查装置的气密性;
(3)根据(1)中的热化学方程式,升温平衡向逆反应方向进行判断;
(4)为使残留在装置中的SO2、SO3被充分吸收,用氧气把装置中的二氧化硫和三氧化硫赶到A装置中吸收三氧化硫,二氧化硫赶入D装置中被氢氧化钠溶液吸收;
(5)依据硫元素守恒计算得到反应生成的三氧化硫物质的量,和剩余二氧化硫被氢氧化钠吸收的物质的量,根据转化率概念计算;结合三氧化硫的物质的量及热化学方程式2SO2(g)+O2(g)═2SO3(g)△H=-196.6kJ/mol计算.
解答 解:(1)Ⅰ装置必须要对二氧化硫进行干燥,可以用浓硫酸来干燥二氧化硫气体;SO3的熔点是16,8℃,可以用冰水来获得三氧化硫;未反应掉的二氧化硫对空气会产生污染,Ⅲ中应该加氢氧化钠溶液尾气处理装置,
故答案为:B;A;D;
(2)实验前,必须进行的操作是检查装置的气密性,
故答案为:检查装置的气密性;
(3)根据(1)中的热化学方程式,升温平衡向逆反应方向进行,所以SO2的转化率会减小,
故答案为:减小;
(4)为使残留在装置中的SO2、SO3被充分吸收,用氧气把装置中的二氧化硫和三氧化硫赶到A装置中吸收三氧化硫,二氧化硫赶入D装置中被氢氧化钠溶液吸收,
故答案为:继续通入氧气一段时间;
(5)已知Ⅱ增加的质量为b g即三氧化硫的质量,因此,反应生成三氧化硫的二氧化硫物质的量=$\frac{bg}{80g/mol}$=$\frac{b}{80}$mol;装置Ⅲ增加的质量为a g即被氢氧化钠吸收的剩余二氧化硫物质的质量,因此,剩余的二氧化硫物质的量=$\frac{ag}{64g/mol}$=$\frac{a}{64}$mol,
所以二氧化硫的转化率=$\frac{\frac{b}{80mol}}{\frac{b}{80}mol+\frac{a}{64}mol}$×100%=$\frac{4b}{4b+5a}$×100%;
反应生成$\frac{b}{80}$mol三氧化硫,根据反应2SO2(g)+O2(g)═2SO3(g)△H=-196.6kJ/mol可知反应放出热量为:196.6kJ/mol×$\frac{1}{2}$×$\frac{b}{80}$mol≈1.223bkJ,
故答案为:$\frac{4b}{4b+5a}$×100%;1.223bkJ.
点评 本题考查工业制硫酸的方法,题目难度中等,涉及二氧化硫的性质、化学平衡的影响因素、计算以及化学方程式的书写等知识,明确实验原理为解答关键,试题综合性较强,充分考查学生分析和解决问题的能力,侧重实验及计算能力的考查.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | D的浓度减小了 | B. | A的转化率减小了 | ||
| C. | 物质B的质量分数增加了 | D. | a+b>c+d |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C2H4O2的有机物不一定有酸性 | |
| B. | 当物质中的化学键发生断裂时,一定发生化学变化 | |
| C. | 等质量的Al分别按a、b两种途径完全转化,途径a比途径b产生的H2多 途径a:Al$\stackrel{HCl}{→}$H2 途径b:Al$\stackrel{Fe_{2}O_{3}}{→}$Fe$\stackrel{HCl}{→}$H2 | |
| D. | 只由一种元素的阳离子与另一种元素的阴离子组成的物质不一定是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
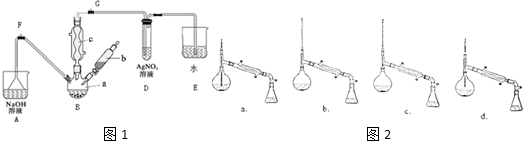
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
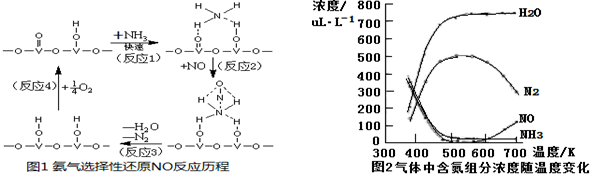
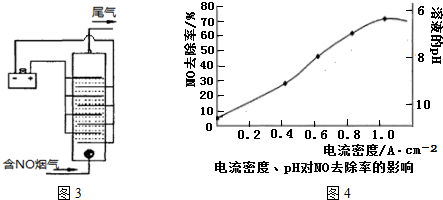
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡时,v正(O2)=v逆(O2)=0必成立 | |
| B. | 关系式5v正(O2)=4v正(NO)总成立 | |
| C. | 在同一段时间范围内,用上述四种物质NH3、O2、NO、H2O的变化表示正反应速率的数值中,v正(H2O)最大 | |
| D. | 若投入4 mol NH3和5 mol O2,通过控制外界条件,必能生成4 mol NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向装置中通入氮气且保持体积不变 | |
| B. | 向装置中通入稍过量氧气且保持体积不变 | |
| C. | 添加更多的催化剂 | |
| D. | 降低温度,及时转移SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用物质 A 表示的反应的平均速率为 0.3 mol•L-1•s-1 | |
| B. | 用物质 B 表示的反应的平均速率为 0.6 mol•L-1•s-1 | |
| C. | 2 s 时物质 A 的转化率为70% | |
| D. | 2 s 时物质 B 的浓度为 0.7 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com