
【题目】下列条件的改变,一定能加快化学反应速率的是
A. 增大压强 B. 升高温度
C. 增大反应物的量 D. 减小生成物的浓度
科目:高中化学 来源: 题型:
【题目】车用妄全气囊中反应方程式为BNaN3=2Na+3N2↑,用双桥线标出电子 转移的数目和变化类型,指出氧化剂和还原剂.若要得到标准状况下33.6LN2 , 需要多少克NaN3(写出计算过程),NaN3的密度约为2g/cm3 , 则NaN3的体积约为多少立方厘米.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4 是一种重要的化工原料,其有关制备途径及性质如图所示。
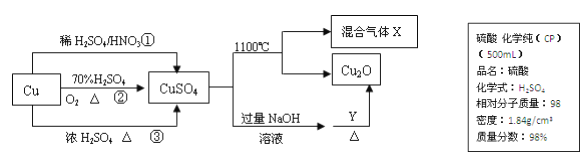
(1)现要用如上图所示的浓硫酸来配制步骤①中所需要的 1mol/L 的稀硫酸 480mL,需用这种浓硫酸的体积为________mL。(保留到小数点后 1 位)
(2)配制该稀硫酸溶液所用到的玻璃仪器除了玻璃棒、量筒、烧杯之外还有_____、_______。
(3)下列哪些操作会使所配的稀硫酸浓度减小________。
A.洗涤烧杯和玻璃棒的溶液未转入容量瓶
B.定容时,眼睛仰视溶液凹液面最低点
C. 容量瓶中原残留少量蒸馏水
D.定容摇匀后容量瓶液面低于刻度线,又加水定容到刻度线
E.量取浓硫酸时量筒内有少量蒸馏水
(4)制取硫酸铜的途径①、②、 ③中,途径______能更好地体现绿色化学思想。
(5)请写出途径③的化学反应方程式________________。
(6)配制 1000mL 0.1mol/L 的硫酸铜溶液,需用托盘天平称取_______g 胆矾。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热化学方程式C(s)+H2O(g) ![]() CO(g)+H2(g);△H=+131.3kJ/mol表示( )
CO(g)+H2(g);△H=+131.3kJ/mol表示( )
A.碳和水反应吸收131.3kJ能量
B.1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C.在298K时,1mol碳(s)和1molH2O(g)反应生成CO(g)和H2(g),吸热131.3kJ
D.1个固态碳原子和1分子水蒸气反应吸热131.1kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中既能跟稀 H2SO4 反应,又能跟 NaOH 溶液反应的有
① Mg ② Al2O3 ③ Al(OH)3 ④ CuCl2
A. ①③ B. ①④ C. ②③ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学平衡常数的说法中,正确的是
A. 在任何条件下,化学平衡常数都是一个定值
B. 当改变反应物的浓度时,化学平衡常数会发生改变
C. 化学平衡常数K与温度、反应物浓度、体系的压强都有关
D. 化学平衡常数K可以推断一个可逆反应进行的程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行反应:2SO2(g)+O2(g) ![]() 2SO3(g).已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.4mol/L、0.2mol/L、0.4mol/L.当反应达到平衡时,可能存在的数据是( )
2SO3(g).已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.4mol/L、0.2mol/L、0.4mol/L.当反应达到平衡时,可能存在的数据是( )
A.SO2为0.8mol/L,O2为0.4 mol/L
B.SO2为0.5 mol/L
C.SO3为0.8 mol/L
D.SO2、SO3均为0.3 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能在溶液中大量共存的是( )
A. Ag+、K+、NO3-、C1- B. Mg2+、Na+、Cl-、SO42-
C. NH4+、Cu2+、OH一、Cl— D. H+、Na+、HCO3-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com