
��100mLBaCl2��AlCl3��FeCl3�Ļ����ҺA�У���μ���Na2SO4��NaOH�Ļ����ҺB�������ij��������ʵ����ͼ�����ҺB�������ϵ��ͼ��ʾ��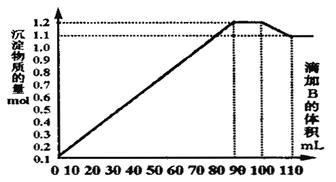
��1��������B��Һ110 mLʱ����Һ�еij����� ���ѧʽ��
��2����A��B��Һ�и����ʵ����ʵ���Ũ�������±���
| �� �� | Na2SO4 | BaCl2 | AlCl3 | FeCl3 |
| /mol��L-1 | | | | |
��1�� BaSO4 Fe(OH)3 ���ѧʽ��
��2���� �� Na2SO4 BaCl2 AlCl3 FeCl3 /mol��L-1 10 10 2 1
��3�� Ba2++SO42-=BaSO4�� Al(OH)3+OH-=AlO2-+2H2O
����������������������߶εĺ��壺����B��Һ0-90mlʱ�����������������������������ᱵ������90-100ml���������ᱵ���������������ܽ⣬���Ҷ������ʵ�����ȣ�100-110ml��ֻ�����������ܽ⣬���ԣ�1��������B��Һ110mlʱ�����������Ѿ��ܽ⣬����Ϊ���ᱵ��������������2������B��Һ100-110ml���ܽ�����������0.1mol�������B��Һ100-110mlʱ��Ҳ�ܽ�����������0.1mol���������ᱵ0.1mol���ɵ��Ȼ�����0.2mol��C��AlCl3��=2mol��L-1������B��Һ0-100mlʱ���ɵ����ᱵ1mol��C��Na2SO4��=10mol��L-1��C��BaCl2��=10mol��L-1��n[Fe��OH��3]=1.1mol-1mol=0.1mol,�ɵ�C��FeCl3��=1mol��L-1��
���㣺���⿼�����ӷ�Ӧ��ͼ���Լ���ѧ���㡣


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��24.4gNaOH��������ˮ,���100mL��Һ,���ܶ�Ϊ1.22g/mL����ش���������
��1������Һ��NaOH�����ʵ���Ũ��Ϊ__________������Һ��NaOH����������Ϊ____________��
��2���Ӹ���Һ��ȡ��10mL������NaOH�����ʵ���Ũ��Ϊ__________��NaOH����������Ϊ___________����Һ���ܶ�Ϊ____________����NaOH������Ϊ___________����NaOH�����ʵ���Ϊ_________��
��3����ȡ����10mL��Һ��ˮϡ�͵�100ml��ϡ�ͺ���Һ��NaOH�����ʵ���Ũ��Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����˵���У���ȷ����
A 1 mol �� B 1. 5mol H2O
C 2 mol ���� D 3 mol ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
2008��5���ҹ��봨���������ֺ���������������������Ա��Ϊ����0.01 mol/L��KMnO4����Һ�����в�������������ҺŨ��ƫ�ߵ���
| A��ȡKMnO4��Ʒʱ�����ڱ���մ�˵�����ˮ |
| B���ܽ����ʱ��Һ��ɽ� |
| C������ʱ��������ƿ�̶��� |
| D��ҡ�Ⱥ��Һ���½����ټ�ˮ���̶��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��NA��ʾ�����ӵ�������ֵ������˵����ȷ����
| A����״���£�22.4 L H2O�к��еķ�����ΪNA |
| B��28 g N2�к��еķ�����ΪNA |
| C��1 mol Mg������ϡ���ᷴӦת�Ƶĵ�����ΪNA |
| D��1 L 1 mol��L��1 Na2 CO3��Һ�к��е���������ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�ҹ���ѧ�ҵ����·��ֽ��10��������٤���������������һ�����⣬�Ƕ���٤�����������dz��м�ֵ�Ĺ��ף�����NA��ʾ�����ӵ�������ֵ��������������ȷ����( )
| A��1mol BrCl��H2O��ȫ��Ӧ�����Ȼ���ʹ����ᣬת�Ƶ�����ΪNA |
| B��п��һ��Ũ�ȵ�Ũ���ᷴӦ��������״����SO2��H2�Ļ������22.4Lʱ��пʧȥ������Ϊ2NA |
| C��1mol CO2�����У��Ҽ��ͦм��ĸ�������2NA |
| D�����³�ѹ�£�14����ϩ����ϩ�Ͷ�ϩ�Ļ����������ԭ����Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ԭ������ԭ����16Oԭ��������ʮ����֮һΪ����������12Cԭ��������ʮ����֮һΪ�����������0.0043%�������ֱ�����ֵ��ͬ����
| A��14N�������� | B���ԭ�ӵ�������� |
| C����Ԫ�ص����ԭ������ | D�������Ƶ�Ħ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����ʱ��ʵ�����ォ1.12 L H2S(g)ͨ��1LijŨ�ȵ��ռ���Һ�У�ǡ����ȫ��Ӧ�����
��Һ��pH=10������仯���Բ��ƣ�����ȷ���ƶ��ǣ�NA���������ӵ�������
| A������ķ�����ĿԼΪ0.05NA�� | B��ԭ�ռ���Һ��Լ��������0.1NA�� |
| C����Ӧ����Һ��Լ��OH- 1��10-4NA�� | D����Ӧ����Һ��Լ��S2- 0.05NA�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��NAΪ�����ӵ�������������������ȷ���ǣ� ��
| A��ͬ��ͬѹ�£�ԭ������ΪNA�������ͺ���������ͬ����� |
| B�������£�21.0g��ϩ�Ͷ�ϩ�Ļ�������к��е�̼ԭ����ĿΪ1.5NA |
C�����³�ѹ�£�1mol����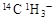 ���������������͵������ֱ�Ϊ8NA��9NA ���������������͵������ֱ�Ϊ8NA��9NA |
| D�����ܱ������м���28g N2��6g H2���ڸ��¡���ѹ�������������³�ַ�Ӧ�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com