
| A. | CH3COONa溶液显碱性 | |
| B. | CH3COOH能与氨水发生中和反应 | |
| C. | 室温下,0.1mol/L的CH3COOH溶液的PH为3 | |
| D. | 相同条件下,等浓度的醋酸溶液的导电能力比盐酸弱 |
分析 要证明醋酸为弱酸,可证明存在电离平衡、不能完全电离或从对应的强碱盐溶液呈碱性的角度,以此解答该题.
解答 解:A.醋酸钠溶液呈碱性,说明醋酸根离子发生了水解,则醋酸为弱酸,能说明醋酸是弱电解质,故A不选;
B.CH3COOH能与氨水发生中和反应,只能说明呈酸性,不能证明为弱酸,故B选;
C.室温下,0.1mol/L的CH3COOH溶液的PH为3,说明醋酸不能完全电离,为弱酸,故C不选;
D.盐酸为强酸,相同条件下,等浓度的醋酸溶液的导电能力比盐酸弱,说明醋酸不能完全电离,为弱酸,故D不选.
故选B.
点评 本题考查了弱电解质的判断,为高频考点,侧重考查学生的分析能力,题目难度不大,电解质强弱是根据其电离程度划分的,不能根据溶液导电性强弱以及与碱的中和反应划分,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 8g | B. | 9g | C. | 12g | D. | 13.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23gNa与O2完全反应,生成Na2O和Na2O2的混合物,转移的电子数为NA | |
| B. | 88.0g14CO2与14N2O的混合物中所含中子数为44NA | |
| C. | 0.1L,l.0mol/L的NaAlO2水溶液中含有的氧原子数为0.2NA | |
| D. | 室温下,将1mol铁片投入到0.5L,18.4mol/L的硫酸中,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
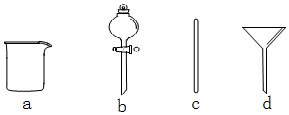
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 足量Mg与2.8gN2完全反应后失去0.2NA电子 | |
| B. | 3.0g由葡萄糖和冰醋酸组成的混合物中含有的原子总数为0.3NA | |
| C. | 常温常压下,2.8gC2H4含有共用电子对的数目为0.6NA | |
| D. | 16gO2含有NA个18O原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 24:30 | B. | 60:24 | C. | 2:1 | D. | 1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com