
| 553~573K |
| 1373K |
| △C |
| t |
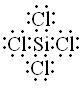 ,SiCl4分子结构对称是非极性分子,故答案为:
,SiCl4分子结构对称是非极性分子,故答案为: ;非极性;
;非极性;| △C |
| t |
| 2a-b |
| t |
| 2a-b |
| 2t |
| 2a-b |
| 2t |


科目:高中化学 来源: 题型:
| A、硅酸钠可用于制备木材防火剂 | B、硅单质广泛用于光纤通讯 | C、利用盐酸刻蚀石英制作艺术品 | D、水晶项链是硅酸盐制品 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硅单质可用来制造太阳能电池 | B、装碱性溶液的玻璃试剂瓶不能用玻璃塞 | C、二氧化硅是制造光导纤维的材料 | D、二氧化硅属于酸性氧化物,不能与任何酸反应 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年上海市普陀区高三上学期质量调研化学试卷(解析版) 题型:填空题
硅及其化合物广泛应用于太阳能的利用、光导纤维及硅橡胶的制备等。
纯净的硅是从自然界中的石英矿石(主要成分为SiO2)中提取的。高温下制取纯硅有如下反应(方法1):
①SiO2(s)+2C(s) Si(s)+2CO(g)
Si(s)+2CO(g)
②Si(s)+2Cl2(g) SiCl4(g)
SiCl4(g)
③SiCl4(g)+2H2(g) →Si(s)+4HCl(g)
完成下列填空:
(1)硅原子核外有 种不同能级的电子,最外层的p电子有 种自旋方向。
(2)硅与碳同主族,单质的还原性:碳 硅(填写“同于”、“强于”或“弱于”)。反应①之所以能进行的原因是 。
(3)反应②生成的化合物的电子式为 ;该分子为 分子(填写“极性”或“非极性”)。
(4)某温度下,反应②在容积为V升的密闭容器中进行,达到平衡时Cl2的浓度为a mol/L。然后迅速缩小容器容积到0.5V升,t秒后重新达到平衡,Cl2的浓度为b mol/L。则:a b(填写“大于”、“等于”或“小于”)。
(5)在t秒内,反应②中v(SiCl4)= (用含a、b的代数式表示)。
(6)工业上还可以通过如下反应制取纯硅(方法2):
④Si(粗) +3HCl(g) 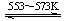 SiHCl3(l)+H2(g) + Q(Q>0)
SiHCl3(l)+H2(g) + Q(Q>0)
⑤SiHCl3(g)+H2(g) Si(纯)+3HCl(g)
Si(纯)+3HCl(g)
提高反应⑤中Si(纯)的产率,可采取的措施有: (选填2条)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com