
下列说法正确的是( )
|
| A. | 活化分子之间的碰撞一定是有效碰撞 |
|
| B. | 反应物分子的每次碰撞都能发生化学反应 |
|
| C. | 升高温度时,活化分子百分数增加 |
|
| D. | 有气体参加的化学反应,增大压强,反应速率增大 |
| 化学反应速率的影响因素. | |
| 专题: | 化学反应速率专题. |
| 分析: | 一般来说,升高温度,活化分子的百分数增大,活化分子之间发生碰撞生成新物质时的碰撞为有效碰撞,如增大压强,气体的浓度增大时,反应速率增大,否则反应速率不变,以此解答. |
| 解答: | 解:A.活化分子之间发生碰撞,生成新物质时的碰撞为有效碰撞,故A错误; B.反应物发生有效碰撞时才能发生化学反应,故B错误; C.升高温度,更多的分子吸收能量,成为活化分子,活化分子百分数增加,故C正确; D.有气体参加的化学反应,增大压强,反应速率不一定增大,如通入惰性气体,故D错误. 故选C. |
| 点评: | 本题综合考查化学反应速率的影响,为高频考点,侧重于基础知识的综合理解和运用的考查,注意影响化学反应的因素以及相关概念的理解,难度不大. |


科目:高中化学 来源: 题型:
粗盐中含可溶性CaCl2、MgCl2及Na2SO4,除去这些杂质的试剂可选用①Na2CO3、②NaOH、③BaCl2、④HCl,加入的先后顺序可以是()
A. ①②③④ B. ②③①④ C. ②①③④ D. ①③②④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述或表示方法正确的是( )
A.伴有能量变化的物质变化都是化学变化
B.0.5 mol H2完全燃烧生成水蒸气放出热量121 kJ,H2燃烧的热化学方程式表示为:2H2(g)+O2(g)===2H2O(g) ΔH=-242 kJ·mol-1
C.由C(金刚石)===C(石墨) ΔH=-1.90 kJ·mol-1,可知石墨比金刚石稳定
D.一个化学反应中,当生成物能量大于反应物能量时,反应放热,ΔH为“-”
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化过程,属于放热反应的是( )
①液态水变成水蒸气
②酸碱中和反应
③浓H2SO4稀释
④固体NaOH溶于水
⑤H2在Cl2中燃烧
⑥弱酸电离.
|
| A. | ②③④⑤ | B. | ②③④ | C. | ②⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨反应N2+3H2 2NH3,某段时间内的平均反应速率分别用v(N2)、v(H2)、v(NH3)表示(单位均为mol•L﹣1•s﹣1)时,下列关系式中正确的是( )
2NH3,某段时间内的平均反应速率分别用v(N2)、v(H2)、v(NH3)表示(单位均为mol•L﹣1•s﹣1)时,下列关系式中正确的是( )
|
| A. | v(H2)=3v(N2) | B. | v(N2)=2v(NH3) | C. | v(NH3)=v(H2) | D. | v(H2)=v(NH3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:①101kPa时,C(s)+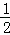 O2(g)=CO(g);△H1=﹣110.5kJ/mol②稀溶液中,H+(aq)+OH﹣(aq)=H2O(1);△H2=﹣57.3kJ/mol,下列结论正确的是( )
O2(g)=CO(g);△H1=﹣110.5kJ/mol②稀溶液中,H+(aq)+OH﹣(aq)=H2O(1);△H2=﹣57.3kJ/mol,下列结论正确的是( )
|
| A. | 若碳的燃烧热用△H3来表示,则△H3<△H1 |
|
| B. | 若碳的燃烧热用△H3来表示,则△H3>△H1 |
|
| C. | 稀硫酸与稀NaOH溶液反应的中和热△H=﹣57.3kJ/mol |
|
| D. | 浓硫酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高一上学期期末考试化学试卷(解析版) 题型:计算题
有一种白色粉末是无水碳酸钠和碳酸氢钠的混合物,称取0.442g灼烧至恒重,把放出的气体通入足量澄清石灰水中,生成0.200g沉淀,灼烧后的残渣能与30mL盐酸恰好完全反应。试求:(1)原混合物中各物质的质量。(2)所用盐酸的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源:2014-2015宁夏银川市高一下学期3月月考化学试卷(解析版) 题型:推断题
(14分)下图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D、E为无色气体,C能使湿润的红色石蕊试纸变蓝,B常温下为无色液体,X是一种酸式盐。
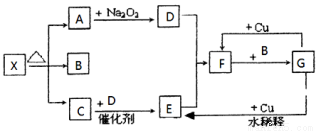
(1)写出下列各物质的化学式:X: ;F: ;G: 。
(2)利用Na2O2与A反应常作供氧剂,写出其反应方程式: 。写出G→E的化学反应方程式: 。
(3)E→F的实验现象是 ,G的稀溶液与少量Fe粉反应的离子方程式为 ,检验反应后溶液中金属阳离子的试剂为 ,实验现象为 。
(4)F→G的反应 (填是或不是)氧化还原反应,若是,则氧化产物是 ,若不是,则此空不填。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com