


 、
、 ;
; +H2O→
+H2O→ +H2SO4;
+H2SO4; +2NaOH→
+2NaOH→ +2NaCl+H2O,写出H发生银镜反应的离子方程式
+2NaCl+H2O,写出H发生银镜反应的离子方程式 +2Ag(NH3)2++2OH-→
+2Ag(NH3)2++2OH-→ +NH4++2Ag↓+3NH3+H2O.
+NH4++2Ag↓+3NH3+H2O. 分析 结合产物的结构简式,利用流程图和起始原料的结构简式以及核磁共振氢谱表明A中有4种氢,知A为 ,A→B是对甲基苯磺酸的硝化反应,生成的B为
,A→B是对甲基苯磺酸的硝化反应,生成的B为 ,B在酸性条件下水解生成C且C的化学式为C7H7NO2,可知C为
,B在酸性条件下水解生成C且C的化学式为C7H7NO2,可知C为 ,C在Fe+HCl条件下发生还原反应生成的D的结构简式为
,C在Fe+HCl条件下发生还原反应生成的D的结构简式为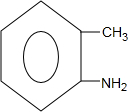 ,D在溴水中发生苯环上-NH2邻对位的取代反应生成E,E在光照条件下与氯气发生甲基上的取代反应,生成的F有三种可能,1取代、2取代、3取代,其1氯取代物与X反应生成的生成物与HCl反应生成沐舒坦,据沐舒坦的结构简式可知,X物质的结构简式为:
,D在溴水中发生苯环上-NH2邻对位的取代反应生成E,E在光照条件下与氯气发生甲基上的取代反应,生成的F有三种可能,1取代、2取代、3取代,其1氯取代物与X反应生成的生成物与HCl反应生成沐舒坦,据沐舒坦的结构简式可知,X物质的结构简式为: ,据此分析.
,据此分析.
解答 解:结合产物的结构简式,利用流程图和起始原料的结构简式以及核磁共振氢谱表明A中有4种氢,知A为 ,A→B是对甲基苯磺酸的硝化反应,生成的B为
,A→B是对甲基苯磺酸的硝化反应,生成的B为 ,B在酸性条件下水解生成C且C的化学式为C7H7NO2,可知C为
,B在酸性条件下水解生成C且C的化学式为C7H7NO2,可知C为 ,C在Fe+HCl条件下发生还原反应生成的D的结构简式为
,C在Fe+HCl条件下发生还原反应生成的D的结构简式为 ,D在溴水中发生苯环上-NH2邻对位的取代反应生成E,E在光照条件下与氯气发生甲基上的取代反应,生成的F有三种可能,1取代、2取代、3取代,其1氯取代物与X反应生成的生成物与HCl反应生成沐舒坦,据沐舒坦的结构简式可知,X物质的结构简式为:
,D在溴水中发生苯环上-NH2邻对位的取代反应生成E,E在光照条件下与氯气发生甲基上的取代反应,生成的F有三种可能,1取代、2取代、3取代,其1氯取代物与X反应生成的生成物与HCl反应生成沐舒坦,据沐舒坦的结构简式可知,X物质的结构简式为: ,
,
(1)结合产物的结构简式,利用流程图和起始原料的结构简式以及核磁共振氢谱表明A中有4种氢,知A为 ,据沐舒坦的结构简式可知,X物质的结构简式为:
,据沐舒坦的结构简式可知,X物质的结构简式为: ,故答案为:
,故答案为: ;
; ;
;
(2)B为 ,B在酸性条件下水解生成C且C的化学式为C7H7NO2,可知C为
,B在酸性条件下水解生成C且C的化学式为C7H7NO2,可知C为 ,反应的化学方程式为
,反应的化学方程式为 +H2O→
+H2O→ +H2SO4,
+H2SO4,
故答案为: +H2O→
+H2O→ +H2SO4;
+H2SO4;
(3)D的结构简式为 ,其含苯环的同分异构体有甲基和氨基临间对3种,还有氨基连在甲基上1种,共4种,核磁共振氢谱中峰面积比3:2:2:2的结构是甲基与氨基在对位的结构,结构简式为
,其含苯环的同分异构体有甲基和氨基临间对3种,还有氨基连在甲基上1种,共4种,核磁共振氢谱中峰面积比3:2:2:2的结构是甲基与氨基在对位的结构,结构简式为 ,故答案为:4;
,故答案为:4; ;
;
(4)E在光照条件下与氯气发生甲基上的取代反应,生成的F有三种可能,1取代、2取代、3取代,E生成F的过程中生成的一种副产物G在NaOH水溶液中生成H,H可发生银镜反应,说明G为2取代产物,结构简式为 ,其在NaOH溶液中水解的化学方程式为
,其在NaOH溶液中水解的化学方程式为 +2NaOH→
+2NaOH→ +2NaCl+H2O,
+2NaCl+H2O, 发生银镜反应的离子方程式为
发生银镜反应的离子方程式为 +2Ag(NH3)2++2OH-→
+2Ag(NH3)2++2OH-→ +NH4++2Ag↓+3NH3+H2O,
+NH4++2Ag↓+3NH3+H2O,
故答案为: +2NaOH→
+2NaOH→ +2NaCl+H2O;
+2NaCl+H2O; +2Ag(NH3)2++2OH-→
+2Ag(NH3)2++2OH-→ +NH4++2Ag↓+3NH3+H2O.
+NH4++2Ag↓+3NH3+H2O.
点评 本题考查了有机框图推断以及有机化学方程式的书写,据官能团的性质以及所给流程图正确的判断各物质的结构简式是解题的关键,题目难度较大.


科目:高中化学 来源: 题型:选择题
| A. | 5.40g | B. | 6.25g | C. | 7.85g | D. | 8.10g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. 2AlN+3H2.
2AlN+3H2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 乙醇分子中各化学键如图所示.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )
乙醇分子中各化学键如图所示.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )| A. | 与金属钠反应时,键①断裂 | |
| B. | 在加热和Cu催化下与O2反应时,键①、③断裂 | |
| C. | 与浓硫酸共热发生消去反应时,键②③断裂 | |
| D. | 与乙酸、浓硫酸共热发生酯化反应时,键①断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有N、O、F的分子和含有氢原子的分子间一定存在氢键 | |
| B. | 对于组成和结构相似的分子,其沸点随着相对分子质量的增大一定增大 | |
| C. | 甲醇极易溶于水而CH4难溶于水的原因只是甲醇是极性分子,CH4是非极性分子 | |
| D. | 过氧化氢气化时肯定只破坏分子间作用力和氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,结构式为
,结构式为 ;
; ,结构式为
,结构式为 ;
; ,结构式为
,结构式为 ;
; ,结构式为-O-H;
,结构式为-O-H; ,结构式为[O-H]-.
,结构式为[O-H]-.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com