
�Т١��ڡ��ۡ��ܡ��ݡ��ޡ��ߡ��ࡢ�ᡢ��ʮ��Ԫ�أ�ԭ�������������ᡢ��ڵ������ڣ������Ϊ������Ԫ�ء�
��1�����ڡ��ߡ�������Ԫ�������ڱ������λ������
|
�� |
|
|
|
|
|
|
�� |
�� |
������γɵ�Һ�廯�����dz������ܼ������Ԫ�������ڱ��е�λ���� ����Ԫ�ص�������ĵ���ʽ�� ��������γɵĻ������д��ڵĻ�ѧ���� ����ڡ��ߡ�������Ԫ������������Ӧ��ˮ��������������ǿ��˳���� (�û�ѧʽ��ʾ)���ߡ�������Ԫ���γɵ������Ӱ뾶��С˳���� (�����ӷ�����)��
��2�����ס����������������Ϊ����������Ԫ������ɵĵ��ʻ���Ҽס��ҡ���Ϊ��ɫ���壬��Ϊ����ɫ���塣������ͼ��ʾת����ϵ�Ʋ⣺

��д����Ӧa�Ļ�ѧ����ʽ�� ��
��д�����붡��Ӧ�Ļ�ѧ����ʽ�� ��
��3������ͼ��A��B��C��D��E�ֱ�������10��Ԫ����ɵĵ��ʻ��
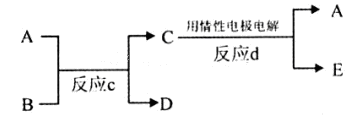
������Ӧc����A�����ص����������B��ˮ��Һ������A�Ǻ�ɫ�������ʣ�E�Ǿ��л���ɫ�����塣��Ӧd�������ĵ缫��ӦʽΪ�� ��
������Ӧc���ڸ����½��еġ�����B�ǰ���ɫ���壬������C��һ�����Ի������Ӧc�Ļ�ѧ����ʽΪ ��
��1���������ڵڢ�A����2�֣�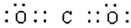 ��1�֣�
��1�֣�
���ۼ���1�֣�H2CO3��H2SO4��HClO4����1�֣�S2�D ��Cl�D ��1�֣�
��2����4NH3��5O2 4NO��6H2O��2�֣�
4NO��6H2O��2�֣�
��3NO2��H2O=2HNO3��NO��2�֣�
��3�� ��Cu2����2e�D=Cu��2�֣�
��2Al��Fe2O3 2Fe��Al2O3��2�֣�
2Fe��Al2O3��2�֣�
��������
�����������1���ڵ�ԭ��������������1���ɢ������ڱ��е�λ�ÿ�֪���ڴ��ڵڶ����ڣ��ߢദ�ڵ������ڣ�������γɵ�Һ�廯�����dz�������Ҫ�ܼ����û�����ΪSC2��CCl4���ɢڢߢ��λ�ÿ�֪����Ϊ̼����Ϊ��Ϊ�ȣ�������γɵ�Һ�廯����ΪCCl4��Sԭ��ԭ����3�����Ӳ㣬����������Ϊ6���������ڱ��е������ڵڢ�A�壻������̼������̼ԭ������ԭ��֮���γ�2�Թ��õ��Ӷԣ�����ʽΪ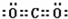 ��CCl4��̼ԭ��������֮���γ�1�Թ��õ��Ӷԣ�Ϊ���ۼ����ǽ�����C��S��Cl������������Ӧˮ���������ǿ����˳����HClO4��H2SO4��H2CO3��S2����Cl�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶S2����Cl������Ϊ���������ڵڢ�A�壻�����ۼ���HClO4��H2SO4��H2CO3��S2����Cl����
��CCl4��̼ԭ��������֮���γ�1�Թ��õ��Ӷԣ�Ϊ���ۼ����ǽ�����C��S��Cl������������Ӧˮ���������ǿ����˳����HClO4��H2SO4��H2CO3��S2����Cl�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶S2����Cl������Ϊ���������ڵڢ�A�壻�����ۼ���HClO4��H2SO4��H2CO3��S2����Cl����
��2����Ϊ����ɫ���壬����ΪNO2����ӦbΪNO+O2��NO2���ɷ�Ӧa��֪�������ҷ�Ӧ���ɱ����ʼ�ΪO2���ʱ�ΪNO����ӦaΪNH3+O2��NO+H2O����ΪNH3����ΪH2O��
�ٷ�Ӧa�Ļ�ѧ����ʽΪ��4NH3+5O2 4NO+6H2O���ʴ�Ϊ��4NH3+5O2
4NO+6H2O���ʴ�Ϊ��4NH3+5O2 4NO+6H2O��
4NO+6H2O��
��NO2��H2O��Ӧ����HNO3��NO����Ӧ����ʽΪ��3NO2+H2O=2HNO3+NO�����ʴ�Ϊ��3NO2+H2O=2HNO3+NO����
��3����A�Ǻ�ɫ�������ʣ�AΪCu��E�Ǿ��л���ɫ�����壬��EΪCl2����Ӧd������������ԭ��Ӧ����ͭ���ӷŵ�����Cu����Ӧd�������缫��ӦʽΪ��Cu2��+2e���TCu��
�ʴ�Ϊ��Cu2��+2e���TCu��
������Ӧc���ڸ����½��еģ�����C��һ�����Ի����ΪAl2O3������B�ǰ���ɫ���壬ΪFe2O3����ӦcΪ���ȷ�Ӧ��AΪAl��DΪFe��EΪO2����Ӧc�ķ���ʽΪ��Fe2O3+2Al 2Fe+Al2O3���ʴ�Ϊ��Fe2O3+2Al
2Fe+Al2O3���ʴ�Ϊ��Fe2O3+2Al 2Fe+Al2O3��
2Fe+Al2O3��
���㣺Ԫ�������ɺ�Ԫ�����ڱ����ۺ�Ӧ�ã�������ƶ�


 ��������ѧ����ϵ�д�
��������ѧ����ϵ�д� ��Ԫ������ĩ��ϵ�д�
��Ԫ������ĩ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
1L��Һ�к����������ӣ���Pt�缫������Һ������·����3mol e-ͨ��ʱ�����Ե��ʱ��Һ����ı仯���缫������ܴ��ڵ��ܽ���������˵����ȷ���ǣ�������
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �л���A������ʳƷ��ҵ����֪9.0g A������O2�г��ȼ�գ������ɵĻ����������ͨ��������Ũ����ͼ�ʯ�ң��ֱ�����5.4g��13.2g��������ʣ������ΪO2��
�л���A������ʳƷ��ҵ����֪9.0g A������O2�г��ȼ�գ������ɵĻ����������ͨ��������Ũ����ͼ�ʯ�ң��ֱ�����5.4g��13.2g��������ʣ������ΪO2��

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com