
【题目】9.03×1023个NH3含_________mol氨分子,_________mol氢原子,__________mol质子,________个电子,在标准状况下的体积为______________L。
【答案】1.54.51515×6.02×102333.6
【解析】
1mol任何物质中含有6.02×1023个分子,则9.03×1023个氨(NH3)分子含氨分子的物质的量为![]() =1.5mol;1个氨分子中含有3个氢原子,则9.03×1023个氨(NH3)分子含1.5mol×3=4.5mol氢原子;1个氢原子中含有1个质子,1个电子,1个氮原子中含有7个质子,7个电子,则1个氨分子中含有10个质子、8个电子,则9.03×1023个氨(NH3)分子含1.5mol×10=15mol质子和电子,标准状况下,所占的体积为1.5mol×22.4L/mol=33.6L,故答案为:1.5;4.5;15;15×6.02×1023;33.6。
=1.5mol;1个氨分子中含有3个氢原子,则9.03×1023个氨(NH3)分子含1.5mol×3=4.5mol氢原子;1个氢原子中含有1个质子,1个电子,1个氮原子中含有7个质子,7个电子,则1个氨分子中含有10个质子、8个电子,则9.03×1023个氨(NH3)分子含1.5mol×10=15mol质子和电子,标准状况下,所占的体积为1.5mol×22.4L/mol=33.6L,故答案为:1.5;4.5;15;15×6.02×1023;33.6。


 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】下面装置是用于FeSO4受热分解及产品检验,已知亚硝酸铵受热易分解,下列相关说法正确的是
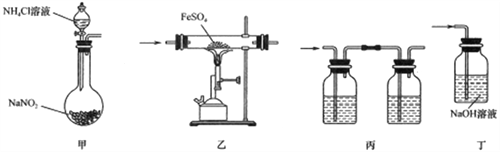
A. 装置甲是N2的制备装置,实验时采用酒精灯直接加热至85℃
B. 点燃装置乙处酒精喷灯前应先通入一段时间N2
C. 装置丙依次装入品红溶液,BaCl2溶液检验产生的气体
D. 采用装置丁,可更好地吸收尾气且避免了尾气外逸污染环境
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最简式相同,但既不是同系物,又不是同分异构体的是
A. 辛烯和3-甲基-1-丁烯 B. 苯和乙炔
C. 1-氯丙烷和2-氯丙烷 D. 甲基环己烷和庚烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度时,将nmol/L氨水滴入10mL1.0mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是( )

A. a点Kw=1.0×10-14
B. 水的电离程度:b>c>a>d
C. b点:c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D. 25℃时,NH4Cl水解常数为(n-1)×10-7(用n表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,有①6.72LCH4,②3.01×1023个HCl,③13.6gH2S ,④0.2molNH3,则下列四种气体的关系表示正确的是()
A. 体积:④<①<②<③ B. 密度:①<③<④<②
C. 质量:④<①<③<② D. 氢原子数:②<③<④<①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法不正确的是
A. 1mol—CH3中含有的质子数为10NA
B. H2O2+Cl2=2HC1+O2反应中,每生成32g O2转移2NA个电子
C. 3.6gCO和 CO2的混合气体含中子数为1.8NA
D. 6.2g 白磷含有0.3NAP-P键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应4CO+2NO2![]() N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
A. υ(CO)=1.5 mol·L-1·min-1 B. υ(NO2)=0.7 mol·L-1·min-1
C. υ(N2)=0.4 mol·L-1·min-1 D. υ(CO2)=1.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸厂周围的空气含有较多二氧化硫,某化学兴趣小组设计了以下装置和方法测定空气(内含N2、O2、SO2、CO2等)中SO2含量。
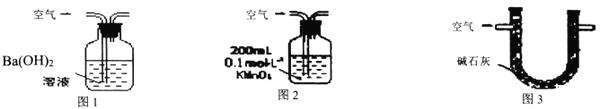
甲.用图1所示装置,通入V升空气,测定生成沉淀的质量
乙.用图2所示装置,当KMnO4溶液刚好褪色时,测定通入空气的体积V
丙.用图3所示装置,通入V升空气,测定U型管增加的质量
(1)你认为可行的操作是________。(填“甲、乙、丙”)
(2)某环保部门为了测定空气中SO2含量,做了如下实验:取标准状况下的空气VL,缓慢通过足量溴水,在所得的溶液中加入过量的氯化钡溶液后,过滤,将沉淀洗涤、干燥,称得其质量为mg。
①若通入气体的速率过快,则测定的SO2的体积分数_______。(选填“偏高”、“偏低”或“不受影响”)。
②如何判断氯化钡溶液已经加过量_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】COS 和H2S 是许多煤化工产品的原料气。已知:
Ⅰ.COS(g)+H2(g)![]() H2S(g)+CO(g) ΔH=X kJ·mol-1;
H2S(g)+CO(g) ΔH=X kJ·mol-1;
I.CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH=-42 kJ·mol-1;
CO2(g)+H2(g) ΔH=-42 kJ·mol-1;
(1)断裂1mol分子中的化学键所需吸收的能量如下表所示:
分子 | COS(g) | H2(g) | CO(g) | H2S(g) | H2O(g) | CO2(g) |
能量/kJ·mol-1 | 1321 | 440 | 1076 | 680 | 930 | 1606 |
则X=_____________________。
(2)向10 L容积不变的密闭容器中充入1mol COS(g)、1mol H2(g)和1mol H2O(g),进行上述两个反应,在某温度下达到平衡,此时CO的体积分数为4%,且测得此时COS的物质的量为0.80mol,则该温度下反应I的平衡常数为_________________(保留两位有效数字)
(3)现有两个相同的2 L恒容绝热(与外界没有热量交换)密闭容器M、N,在M 中充入1mol CO和1molH2O,在N 中充入1molCO2和1molH2,均在700℃下开始按Ⅱ进行反应。达到平衡时,下列说法正确的是_________。
A.两容器中CO 的物质的量M>N
B.两容器中正反应速率M
C.容器M 中CO的转化率与容器N 中CO2的转化率之和小于1
D.两容器中反应的平衡常数M>N
(4)氢硫酸、碳酸均为二元弱酸,其常温下的电离常数如下表:
H2CO3 | H2S | |
Ka1 | 4.4× 10-7 | 1.3×10-7 |
Ka2 | 4.7× 10-11 | 7.1×10-15 |
煤的气化过程中产生的H2S 可用足量的Na2CO3溶液吸收,该反应的离子方程式为______________;常温下,用100mL0.2mol·L-1InaOH溶液吸收448mL(标况)H2S气体,反应后溶液中离子浓度从大到小的顺序为__________________________________。
(5)25℃时,用Na2S沉淀Cu2+、Sn2+两种金属离子 (M2+),所需S2-最低浓度的对数值1gc(S2-)与Igc(M2+

①25℃时Ksp(CuS)=_______________。
②25℃时向50mL的Sn2+、Cu2+浓度均为0.01mol/L的混合溶液中逐滴加入Na2S溶液,当Na2S溶液加到150mL时开始生成SnS沉淀,则此时溶液中Cu2+浓度为_____________mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com