
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源:不详 题型:单选题
A.检验亚硫酸钠试样是否变质:试样 沉淀不溶解 沉淀不溶解 |
B.除去乙酸乙酯中混有的乙酸:混合液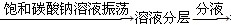 得上层液体 得上层液体 |
C.证明酸性条件下H2O2氧化性比I2强: NaI溶液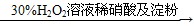 溶液变蓝色 溶液变蓝色 |
| D.鉴定盐A的成分是FeBr2: |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.通入溴水中 | B.将气体点燃 |
| C.通入酸性高锰酸钾溶液中 | D.一定条件下与H2反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.⑤④③②① | B.④③①②⑤ | C.④①②③⑤ | D.②③①④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②一④一①一③一⑤ | B.②一①一③一④一⑤ |
| C.①一③一⑤一②一④ | D.③一①一②一⑤一④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 物质 | 加入试剂 | 操作方法 |
| ①苯(苯甲酸) | | |
| ②乙酸乙酯(乙醇) | | |
 与足量的NaOH溶液充分反应,消耗
与足量的NaOH溶液充分反应,消耗查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com