

| ||
| ||
| ||
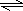 H++Cl-+HClOƽ�������ƶ����ʿ��ñ���ʳ��ˮ��ȥHCl��������ˮ��Ӧ��������ʹ����ᣬ���������Ư���ԣ���ʹ��ɫ������ɫ�����Կ�����������ʪ��ĺ�ɫ������ɫ�������ܺ͵⻯�ط����û���Ӧ���ɵⵥ�ʣ����Կ�������������Һ����ɫ��Ϊ��ɫ��
H++Cl-+HClOƽ�������ƶ����ʿ��ñ���ʳ��ˮ��ȥHCl��������ˮ��Ӧ��������ʹ����ᣬ���������Ư���ԣ���ʹ��ɫ������ɫ�����Կ�����������ʪ��ĺ�ɫ������ɫ�������ܺ͵⻯�ط����û���Ӧ���ɵⵥ�ʣ����Կ�������������Һ����ɫ��Ϊ��ɫ��
| ||
| ||
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʵ������ͨ����MnO2��Ũ���ᷴӦ��ȡ�������䷴Ӧ�Ļ�ѧ����ʽΪ��
MnO2��4HCl��Ũ��![]() Cl2����MnCl2��2H2O
Cl2����MnCl2��2H2O

�Իش��������⣺
��1���÷�Ӧ��������ԭ��Ӧ�𣿢� ����ǡ����ǡ����������������ԭ��Ӧ��ָ������������ ���ۻ�ԭ���� ����д���÷�Ӧ�����ӷ���ʽ ��
��2������ƿA��ʢװ���DZ���ʳ��ˮ��ע�������ڱ���ʳ��ˮ���ܽ�Ⱥ�С������
�����ڱ���ʳ��ˮ�е��ܽ����ܴ��������� ��
��3����������ˮ�����ԣ��������ж������о��ҵĴ̼��ԣ��������������������
����������������β��ֱ����������У�����Ⱦ������ʵ�����пɲ��� ��Һ�������ж���������
��4��һ��ʵ���У�����Ũ����200mL�����ܶ�Ϊ1.19g��cm-3��HCl����������Ϊ36.5%��
��MnO2�պ���ȫ��Ӧʱ��������5.6L����״������������
�Լ����Ũ��������ʵ���Ũ�Ⱥͱ�������HCl�����ʵ���������д��������̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�갲��ʡ����ɽ���и�һ��ѧ���������ʲ��Ի�ѧ�Ծ����������� ���ͣ������
(8��) ʵ������ͨ����MnO2��Ũ���ᷴӦ��ȡ�������䷴Ӧ�Ļ�ѧ����ʽΪ��
MnO2 + 4HCl(Ũ) �� MnCl2 + Cl2��+ 2H2O
��1���ڸ÷�Ӧ�У�����1 mol Cl2���ɣ���������HCl�����ʵ����� mol��ת�Ƶ��ӵ����ʵ����� mol��
��2������ȡCl2ʱΪ��ֹ����Ⱦ������NaOH��Һ����β��.д�������ӷ���ʽ___________.
��3����ֽ�����˶�����������ϴʱ������ʹ�á�����顱����Ҫ�ɷ������ᣩ�롰84����Һ������Ҫ�ɷ���NaClO�����������ж����¼����Ը�����Ļ�ѧ֪ʶ������ԭ���ǣ������ӷ���ʽ��ʾ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ��һ��ѧ����ĩ������ѧ�Ծ���A���������棩 ���ͣ�������
����12�֣�ʵ������ͨ����MnO2��Ũ�����ڼ��ȵ������·�Ӧ��ȡ������Ϊ�����й�����������ʵ�飬��Ҫ4ƿ�ݻ�Ϊ100ml����������״������
��1��д��ʵ������ȡ�����Ļ�ѧ��Ӧ����ʽ���������ת�Ƶķ�����Ŀ��
��2����ȡ4ƿ��������������ҪMnO2����������Ƕ��٣���Ũ��������������Բ��䣩
��3��ʵ�ʳ�����MnO2��������������������������Ҫԭ����ʲô��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com