
在相同温度下,往体积相同的两个密闭容器中通入等质量的CO2和SO2气体,下列说法正确的是
[ ]
A.CO2和SO2的物质的量相同
B.CO2和SO2的密度比为1∶1
C.CO2和SO2的压强比为16∶11
D.CO2和SO2的摩尔质量比为1∶1
科目:高中化学 来源: 题型:
| c(H+)c(HCO-3) |
| c(H2CO3) |
| c(H+)c(HCO-3) |
| c(H2CO3) |
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| KSP | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
查看答案和解析>>
科目:高中化学 来源: 题型:
![]()
①SO2在接触室中反应的平衡转化率与压强、温度的关系如下表(MPa=106Pa):?
 根据化学平衡理论和上表数据,考虑综合经济效益,接触室中的反应压强宜
根据化学平衡理论和上表数据,考虑综合经济效益,接触室中的反应压强宜
选择 MPa;而反应温度选定400~500 ℃的理由是 。?
②往体积相同的甲、乙两个容器中,分别充入等物质的量的SO2和O2,在相同温度下发生反应,反应过程中,甲容器保持体积不变,乙容器保持压强不变,当反应达到平衡时,甲容器中SO2的转化率 (填“>”“=”或“<”)乙容器中SO2的转化率。?
(2)考虑综合经济效益,当炉渣中含铁量大于45%时,可用于炼铁、制造硫酸亚铁等。?
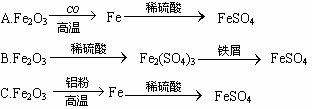
①利用炉渣里的Fe2O3制FeSO4的方案中,最可行的是 (填标号)。?
②FeSO4·7H2O是水处理的常用凝聚剂。净水过程中Fe2+经氧化水解生成 ,净水的原理是 ?
查看答案和解析>>
科目:高中化学 来源:2013届福建省高二第三学段考试化学试卷(解析版) 题型:填空题
(6分)在一定温度下,将2molA和2molB两种气体混合放入体积为2L的密闭刚性容器中,发生如下反应: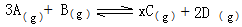
2min末反应达到平衡,生成0.8molD,并测得C的浓度为0.4mol•L-1请回答:
(1)x的值为_______ (2)A的转化率为________
(3)此温度下该反应的平衡常数K=
(4)若在同样的条件下,开始时加入C 、 D 各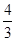 mol,要使平衡时各物质的百分含量与上述平衡相同,则还要加入______mol______ 物质.
mol,要使平衡时各物质的百分含量与上述平衡相同,则还要加入______mol______ 物质.
(5)保持温度不变,往同一容器中通入A、B、C、D各1mol,该反应向 方向移动。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年江苏省高三第一次模拟考试化学试卷 题型:选择题
某可逆反应:a A(g)+b B(g) c C(g)+d D(g) △H = -Q kJ/mol(Q为正值),达平衡状态后,下列结论中不正确的是
A.若a+b=c+d,则往含有w mol气体的平衡体系中再加入w mol的B,达到新平衡时,气体的总物质的量等于2w mol
B.若平衡时,A、B 的转化率相等,说明反应开始时加入的A、B的物质的量之比为 a︰b
C.在相同条件下,两相同容器中分别加入amolA、bmolB和cmolC、dmolD,达到平衡状态后,前者放出热量Q1 kJ,后者吸收热量Q2 kJ,则Q1+ Q2 = Q
D.若温度不变,将容器的体积缩小到原来的一半,A的浓度为原来的1.9倍,则a+b<c+d
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com