
【题目】电子排布有能级顺序,若以E(nl)表示某能级的能量,以下各式中正确的是
A. E(4s)>E(3d)>E(3Px)>E(3Py)
B. E(3d)>E(4s)>E(3p)>E(3s)
C. E(5s)>E( 4f)>E(3Px)=E(3Py)
D. E(5s)>E(4s)>E( 4f)>E(3d)
科目:高中化学 来源: 题型:
【题目】等浓度的下列稀溶液:①乙酸Ka:1.76×10—5、②HClO Ka:2.95×10—8、③碳酸Ka1:4.30×10—7、④乙醇,它们的pH由小到大排列正确的是( )
A. ④②③①B. ③①②④C. ①②③④D. ①③②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有M、A、B、D、N、E六种短周期元素,原子序数依次增大,M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期中最大的,A、B、D、E四种元素在周期表中的相应位置如下图,它们的原子序数之和为37。下列说法不正确的是
![]()
A.A、B、D、E四种元素分别与M元素形成的简单化合物中,稳定性最强的是H2O
B.M、D、E、N形成的简单离子的半径大小:S2>O2>Na+>H+
C.A、B、D、M可组成多种含18电子的分子,如CH3OH、CH3CH3、CH3NH2等
D.B元素的氢化物与D元素的单质在一定条件下能发生置换反应,且氧化剂与还原剂的物质的量之比为4∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对各组物质性质的比较中,正确的是
A. 硬度:Li>Na>K
B. 熔点:NaCl>CaO
C. 电负性:Na<Al<Mg
D. 空间利用率:体心立方堆积<六方堆积<面心立方堆积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组反应中最终肯定是白色沉淀的是( )
A. 单质钠投入 MgCl2溶液 B. AlCl3溶液中加入过量KOH溶液
C. FeCl2溶液中加入过量氨水 D. Fe2(SO4)3溶液中加入过量KOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,反应后固体物质质量减小的是 ( )
A. 二氧化碳通过Na2O2粉末 B. 镁条在二氧化碳中燃烧
C. CO通过灼热的CuO粉末 D. 将铝粉投入CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C4H10O且属于醇类的同分异构体有x种(不包括立体异构,下同),分子式为C5H10O且属于醛类的有机物的同分异构体有y种,则 x和y的关系为( )
A. x=yB. x>yC. x<yD. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是清洁的能源,也是重要的化工原料。
(1)以H2为原料制取氨气进而合成CO(NH2)2的反应如下:
N2(g)+3H2(g)+CO2(g)===CO(NH2)2(s)+H2O(l) ΔH=179.38 kJ·mol1
已知: 2NH3(g)+CO2(g)===NH2CO2NH4(s) ΔH=159.47 kJ·mol1
NH2CO2NH4(s) ===CO(NH2)2(s)+H2O(l) ΔH=+72.49 kJ·mol1
则N2(g)+3H2(g) ===2NH3(g) ΔH= kJ·mol1。
(2)储氢材料领域是当前研究热点,LiBH4是一种良好的储氢材料。采用球磨法制备Al与LiBH4的复合材料,并对AlLiBH4体系与水反应产氢的特性进行下列研究:
①图甲为25℃水浴时每克不同配比的AlLiBH4复合材料与水反应产生H2体积随时间变化关系图。由图可知,下列说法正确的 (填字母)。
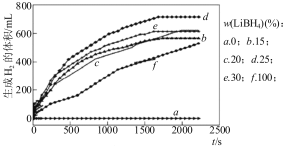

甲 乙
a.25℃时,纯LiBH4和铝均与水反应产生氢气
b.25℃时,复合材料中铝不能产生氢气,只是起到催化作用
c.25℃时,AlLiBH4复合材料中LiBH4含量25%,储氢效果最好
②图乙为25℃和75℃时,AlLiBH4复合材料[ω(LiBH4)=25%]与水反应一定时间后产物的X射线衍射图谱(X射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。从图分析,25℃时AlLiBH4复合材料中LiBH4与水反应生成的LiB(OH)4化学方程式为 ,铝元素的存在有多种形式,其中Al(OH)3产生的原因可能是 。
(3)已知H2S高温热分解制H2的反应为:H2S(g)![]() H2(g)+1/2S2(g)在恒容密闭容器中,控制不同温度进行H2S的分解实验,以H2S的起始浓度均为c mol·L1测定H2S的转化率,结果如下图所示:
H2(g)+1/2S2(g)在恒容密闭容器中,控制不同温度进行H2S的分解实验,以H2S的起始浓度均为c mol·L1测定H2S的转化率,结果如下图所示:

图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则反应速率v(S2)= (用含c、t的代数式表示)。请说明随温度的升高,曲线b向曲线a逼近的原因: 。
(4)用惰性电极电解煤浆液的方法制H2的反应为:C(s)+2H2O(l) ===CO2(g)+2H2(g)现将一定量的1 mol·L1 H2SO4溶液和适量煤粉充分混合,制成含碳量为0.02 g·mL1~0.12g·mL1的煤浆液,置于如图所示装置中进行电解(两电极均为惰性电极)。则B极的电极反应式为 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某烃A的分子组成和结构,对这种烃进行以下实验:
①取一定量的该烃,使其充分燃烧后的气体通过干燥管,干燥管增重7.2g;再通过石灰水,石灰水增重17.6g。
②经测定,该烃(气体)在标准状况下的密度为1.25g·L-1。
现以A为主要原料合成乙酸乙酯,其合成路线如图1所示.

(1)A分子中官能团的名称是___________,0.1mol该烃A能与_______g溴发生加成反应;加成产物需_______mol溴蒸气完全取代。B中官能团的名称是________________;
(2)写出C的结构简式_______________;
(3)反应②的化学方程式是______________________________;
反应④的化学方程式是______________________________;
(4)E是常见的高分子材料,合成E的化学方程式是__________________________。
(5)某同学用如图2所示的实验装置制取少量乙酸乙酯.实验结束后,试管甲中上层为透明的、不溶于水的油状液体.
①实验开始时,试管甲中的导管不伸入液面下的原因是_______________;
②上述实验中饱和碳酸钠溶液的作用是(填字母)_____________;
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
③在实验室利用B和D制备乙酸乙酯的实验中,若用1mol B和1mol D充分反应,不能生成1mol 乙酸乙酯,原因是_____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com