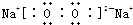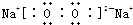元素A、B、C、D、E、F的原子序数依次增大,前五种元素为短周期元素,F元素为第四周期元素,且D、F为常见金属元素.A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g?L
-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):

其中,均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;无论是含有D元素还是含有F元素,相邻的乙与丙或丙与丁两两间互不发生化学反应.请回答下列问题:
(1)写出化合物甲的电子式:
.
(2)写出化合物甲的水溶液与D元素对应的金属阳离子反应的离子方程式
;写出均含有F元素的乙与丁在溶液中发生反应的离子方程式
.
(3)复盐是指由2种或2种以上阳离子和一种阴离子组成的盐.请写出由A、B、C、E、F元素组成的一种具有还原性的复盐戊的化学式
.化合物己是制备复盐戊的必须物质之一,工业上常用氧气、水和FE
2来制取,并得到E的高价态化合物,请写出工业上由FE
2制取化合物己的化学方程式
.
(4)EC
2是啤酒中含量较低而又重要的组分,大部分是在发酵过程中产生的,是啤酒内源抗氧化物的一种,它的存在量与啤酒的抗氧化性有很大的关系.图2是某啤酒样品不同时间段总EC
2的变化情况,请运用所学的知识解释啤酒样品中总EC
2随时间变化的主要原因是
.
(5)由A、C元素组成化合物庚和A、E元素组成的化合物辛,式量均为34.其中庚的熔沸点高于辛,其原因是:
.


 ,
, ;
;

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案 短周期元素A、B、C、D、E、F原子序数依次增大,A与C可形成A2C2和A2C两种化合物;B的最高价氧化物对应的水化物甲与气体BA3化合生成离子化合物乙;D与A位于同一主族:E与C形成的化合物是大气污染物,容易形成酸雨;F元素最高化合价与最低化合价的代数和为6.
短周期元素A、B、C、D、E、F原子序数依次增大,A与C可形成A2C2和A2C两种化合物;B的最高价氧化物对应的水化物甲与气体BA3化合生成离子化合物乙;D与A位于同一主族:E与C形成的化合物是大气污染物,容易形成酸雨;F元素最高化合价与最低化合价的代数和为6.