
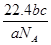 L (2)m:n n:m
L (2)m:n n:m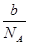 mol,相对分子质量为
mol,相对分子质量为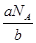 。则c克该气体物质的量为
。则c克该气体物质的量为 =
=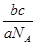 mol,故其在标准状况下的体积是
mol,故其在标准状况下的体积是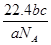 L。
L。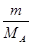 =
=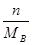 ,可推出
,可推出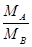 =
=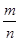 。同温同压下,密度之比等于摩尔质量之比,故A与B在标况下的密度之比为m:n;同质量的气体A与B的分子数之比为(
。同温同压下,密度之比等于摩尔质量之比,故A与B在标况下的密度之比为m:n;同质量的气体A与B的分子数之比为( ):(
):( )=
)=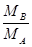 = n:m。
= n:m。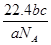 L (2)m:n n:m
L (2)m:n n:m

 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源:不详 题型:单选题

| A.Mg、Al均过量 |
| B.Mg、Al均不足,硫酸过量 |
| C.Ⅱ表示Mg与稀H2SO4反应 |
| D.产生氢气的速率是Ⅰ大于Ⅱ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1mol O2中约含有12.04×1023个氧原子,在标准状况下占有体积约22.4L |
| B.1mol O3和1.5mol O2含有相同的氧原子数 |
| C.1mol Cl2与足量钠反应,转移的电子为2 mol |
| D.相同条件下,N2和O3的混合气体与等体积的N2所含原子数相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.9g重水所含有的电子数为5NA |
| B.1molMgCl2中含有离子数为NA |
| C.1molC10H22分子中共价键总数为31NA |
| D.7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.M g | B.1/M g |
| C.M/6.02×1023g | D.6.02×1023/M g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.49% | B.小于49% | C.大于49% | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com