
工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3气体,已知该反应为放热反应。现将2 mol SO2、1 mol O2充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO2的转化率为50%,则下列热化学方程式正确的是
A.2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
B.2SO2(g)+O2(g) 2SO3(g) ΔH=-98.3 kJ·mol-1
2SO3(g) ΔH=-98.3 kJ·mol-1
C.SO2(g)+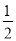 O2(g)
O2(g) SO3(g) ΔH=+98.3 kJ·mol-1
SO3(g) ΔH=+98.3 kJ·mol-1
D.SO2(g)+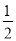 O2(g)
O2(g) SO3(g) ΔH=-196.6 kJ·mol-1
SO3(g) ΔH=-196.6 kJ·mol-1
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源:2016届安徽省高三上学期期中测试化学试卷(解析版) 题型:选择题
现有H2SO4、BaCl2、K2CO3、FeSO4和氯水五种溶液,有如图所示的相互关系,图中每条连线两端的物质可以发生化学反应。下列推断不合理的是

A.X一定为H2SO4 B.Y一定为K2CO3
C.Z可能是氯水 D.M可能为FeSO4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省台州市高一上学期第一次月考化学试卷(解析版) 题型:选择题
物质发生化学变化时:①电子总数 ②原子总数 ③分子总数 ④物质的种类 ⑤物质的总质量 ⑥物质的总能量,反应前后肯定不发生变化的是
A. ①③⑤ B. ①②⑤ C. ①⑤⑥ D. ①④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西省高一上学期期中测试化学试卷(解析版) 题型:填空题
完成下列各题:
(1)在18.6g Fe和Zn合金中加入200mL某浓度的稀硫酸恰好完全反应,生成0.3mol H2.则原合金中有__________mol Fe,稀硫酸的物质的量浓度为__________ mol/L.
(2)已知19.2gCu与过量的200ml 5mol/L稀硝酸充分反应,反应方程式如下,请计算(忽略反应前后溶液体积的变化).3Cu+8HNO3 3Cu(NO3)2+2NO↑+4H2O
3Cu(NO3)2+2NO↑+4H2O
①转移电子的个数为__________(用NA表示阿伏加德罗常数);标准状况下,产生NO气体的体积为__________.
②反应后,H+的物质的量浓度为__________,NO3﹣的物质的量浓度为__________.
查看答案和解析>>
科目:高中化学 来源:2016届北京市高三上学期期中测试化学试卷(解析版) 题型:选择题
为实现下列实验目的,所用试剂合理的是
选项 | 实验目的 | 试剂 |
A | 验证Br2的氧化性强于I2 | 溴水、KI溶液、淀粉溶液 |
B | 除去Fe2O3中的Al2O3 | 稀盐酸 |
C | 检验Fe3O4溶于盐酸后的金属阳离子 | NaOH溶液 |
D | 制备Fe(OH)3胶体 | 饱和FeCl3溶液、NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源:2016届宁夏大学附属中学高三上学期第三次月考理综化学试卷(解析版) 题型:填空题
(1)某可逆反应在不同条件下的反应历程分别为 、
、 ,如图所示。
,如图所示。

①据图判断该反应是 (填“吸”或“放”)热反应,当反应达到平衡后,其他条件不变,升高温度,反应物的转化率 (填“增大”、“减小”或“不变”);
②其中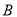 历程表明此反应采用的条件为 (选填序号)。
历程表明此反应采用的条件为 (选填序号)。
A.升高温度 B.增大反应物的浓度 C.降低温度 D.使用催化剂
(2)1000℃时,硫酸钠与氢气发生下列反应:
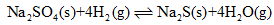
该反应的平衡常数表达式为 。
已知K1000℃ < K1200℃, 若降低体系温度,混合气体的平均相对分子质量将 (填“增大”、“减小”或“不变”)
(3)生铁在潮湿空气中会发生吸氧腐蚀。
①电解质溶液可选用(填序号) 。
A.NaOH溶液 B.C2H5OH C.NaCl溶液 D.稀硫酸
②写出生铁在潮湿空气中吸氧腐蚀正极的电极反应式 。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省杭州市七校高三上学期期中联考化学试卷(解析版) 题型:选择题
下列有关化学用语表达正确的是:
A.质子数为92、中子数为146的U原子: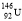
B. HClO的结构式:H-Cl-O
C.HF的电子式: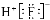
D. 35Cl-和37Cl-离子结构示意图均可以表示为: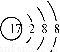
查看答案和解析>>
科目:高中化学 来源:2016届宁夏育才中学高三上学期第四次月考化学试卷(解析版) 题型:实验题
氢化钙固体是登山运动员常用的能源提供剂。某兴趣小组拟选用如下装置制备氢化钙。

请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为___ _____(填仪器接口的字母编号)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞;下一步操作是:_________(填序号)。
A.加热反应一段时间 B.收集气体并检验其纯度
C.关闭分液漏斗活塞 D.停止加热,充分冷却
(3)实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色,该同学据此断,上述实验确有CaH2生成。
①写出CaH2与水反应的化学方程式______ ___________
②该同学的判断不正确,原因是______ ___________(用化学方程式表示)
(4)登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com